08. Tumor de Células Gigantes do Rádio – Técnica de ressecção do tumor – Técnica de obtenção do enxerto autólogo da fíbula – Técnica de reconstrução do punho


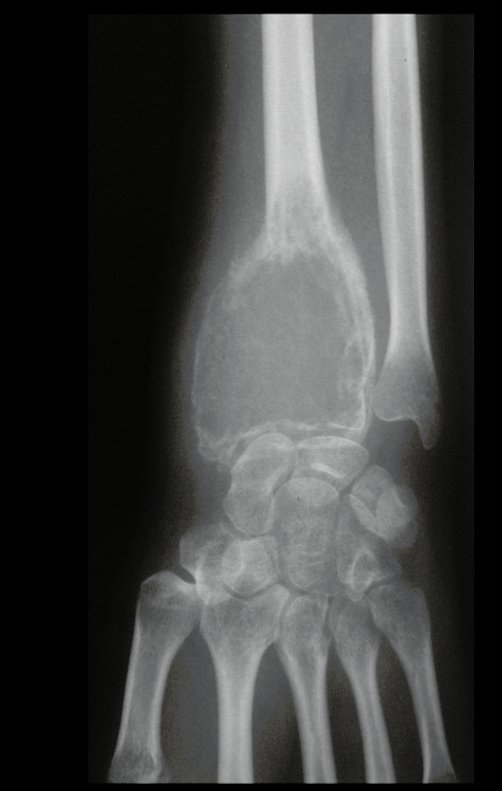
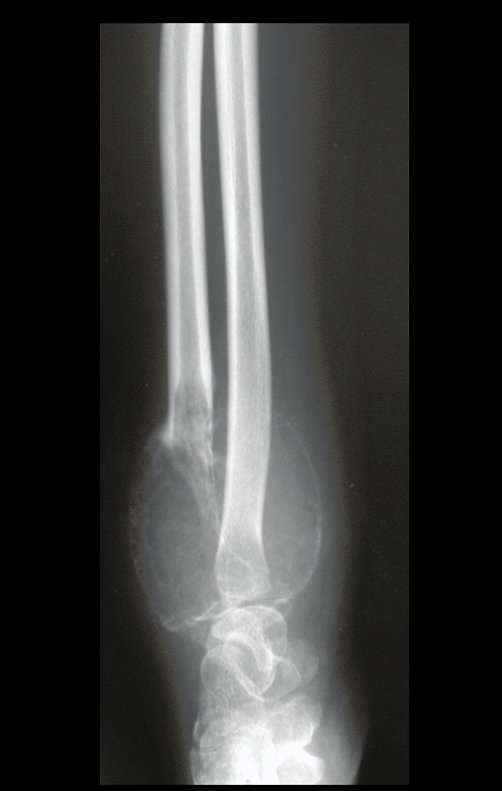
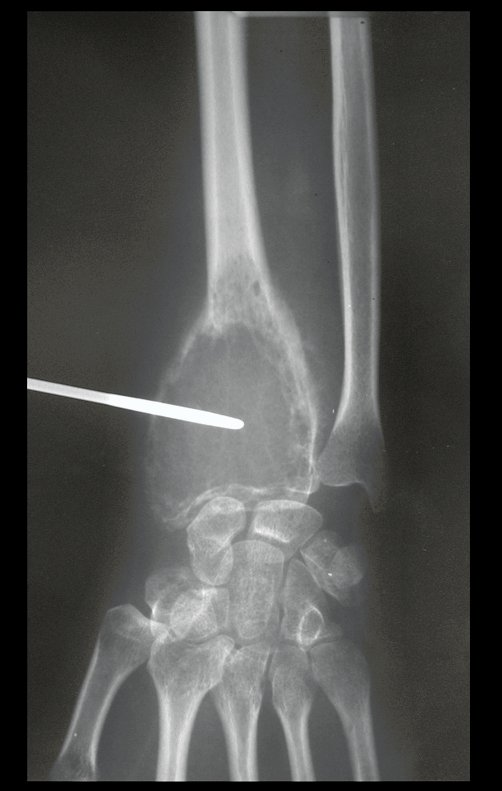
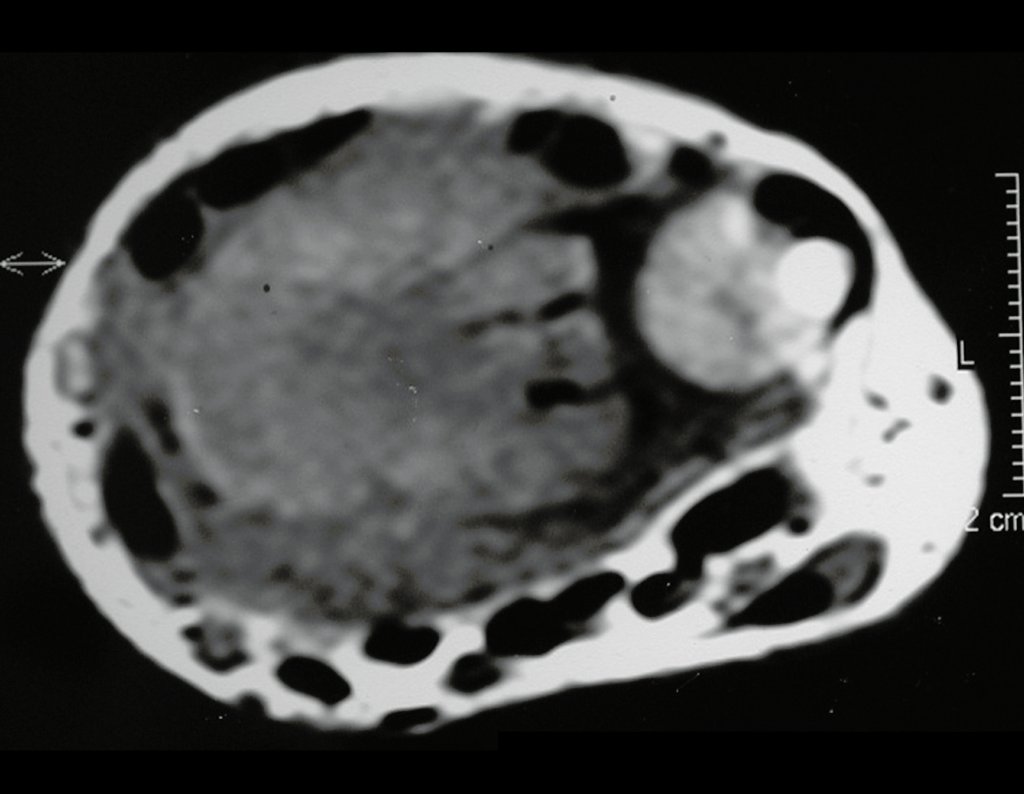
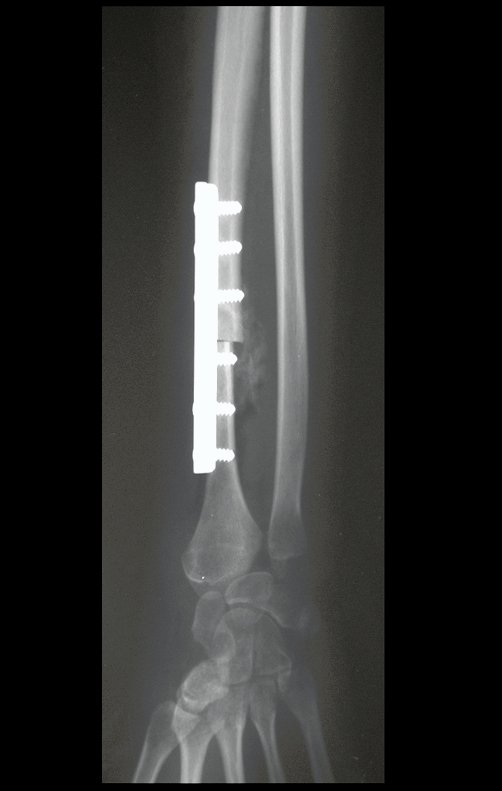
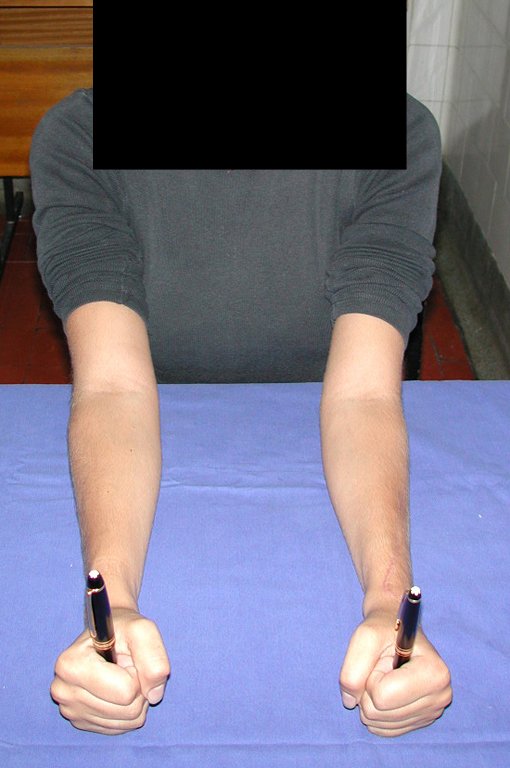
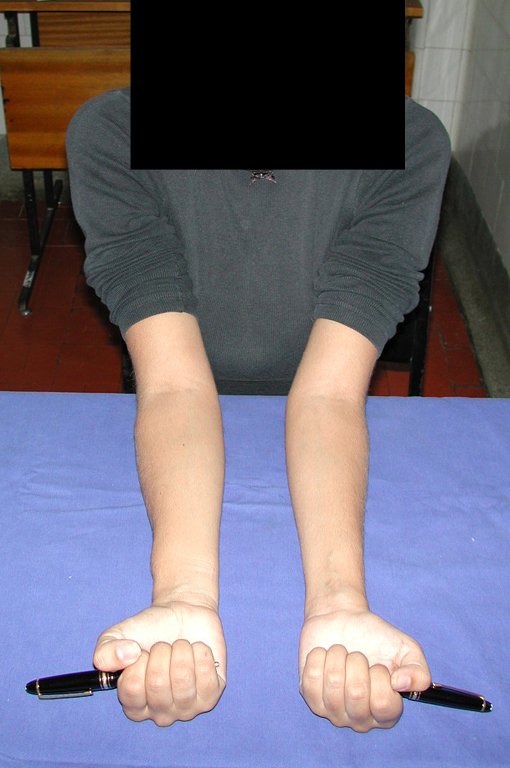
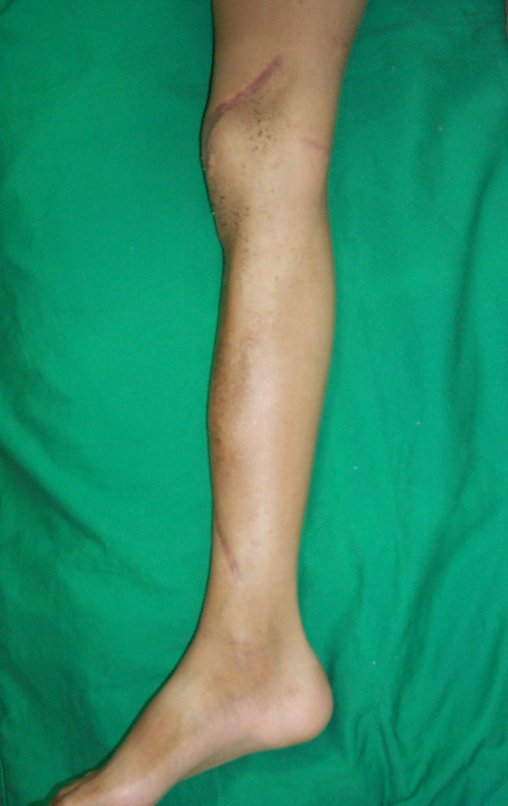
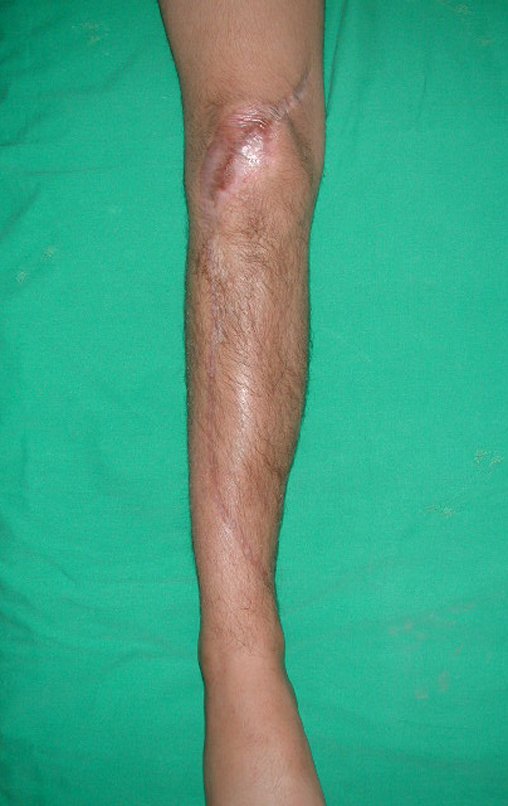
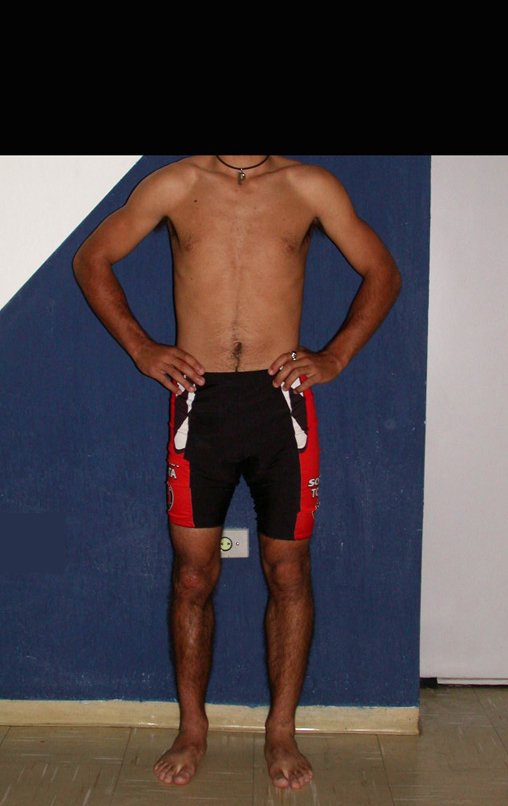
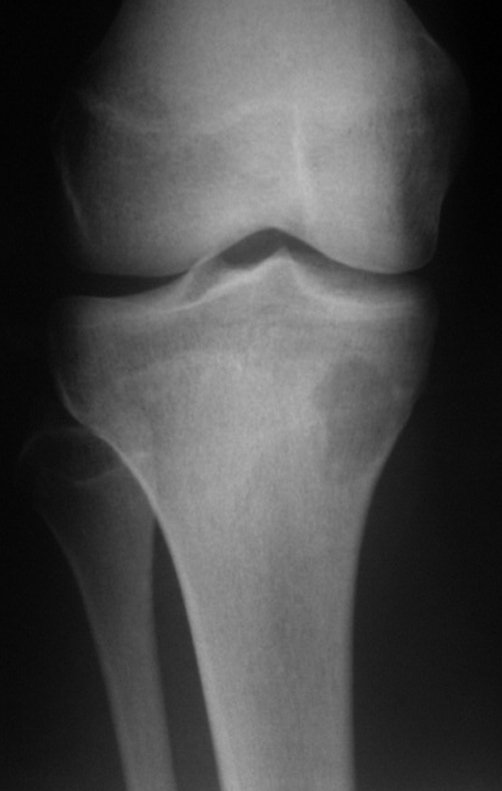
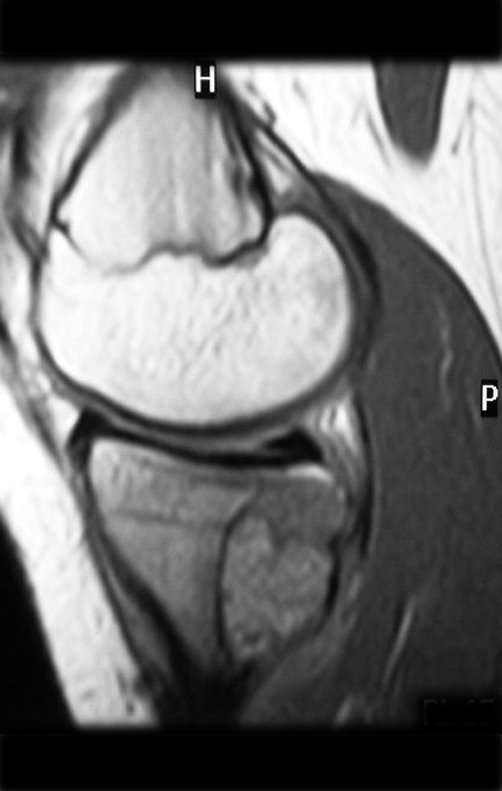
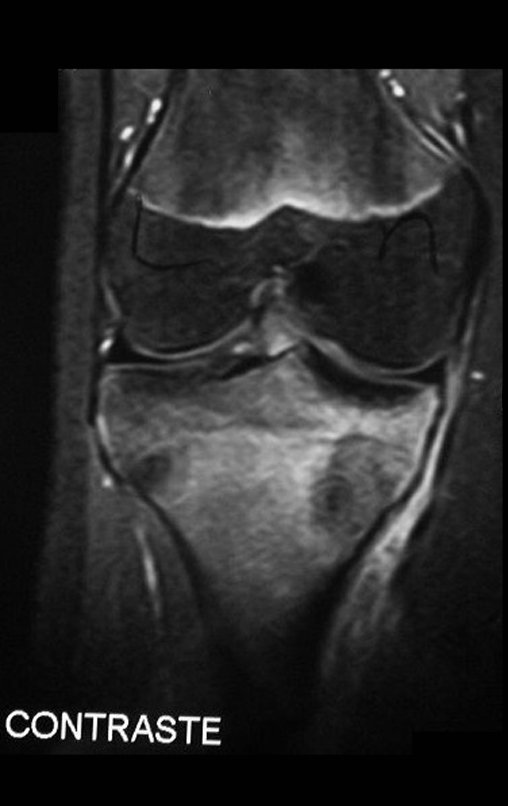
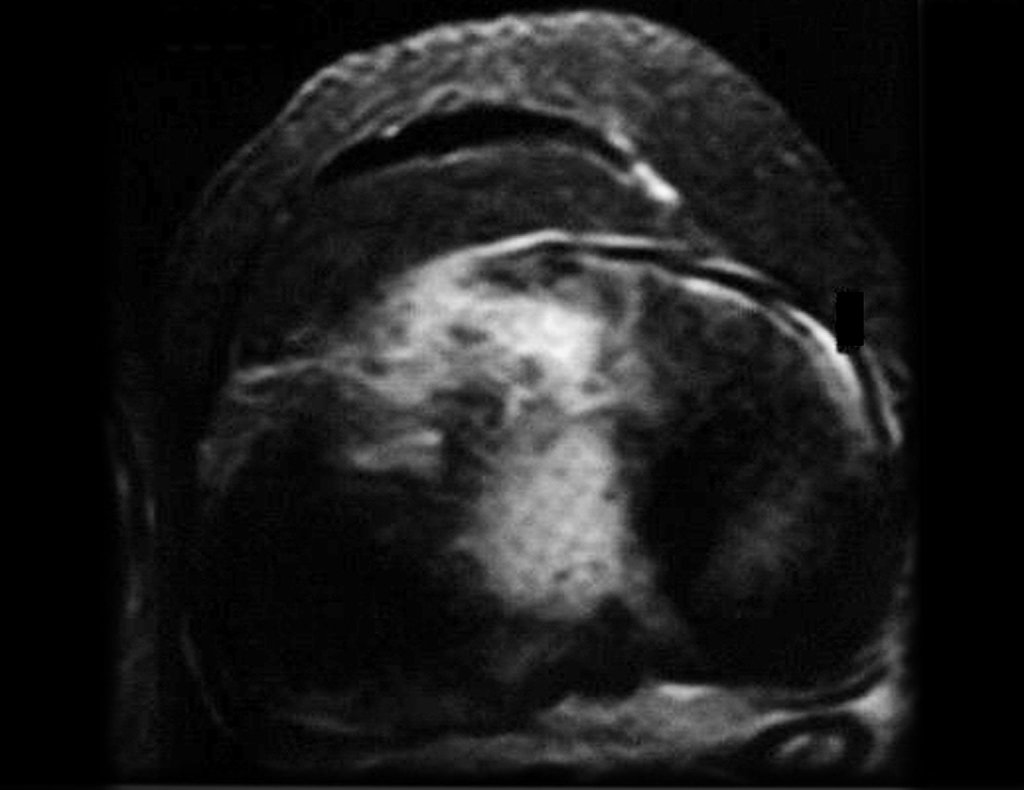
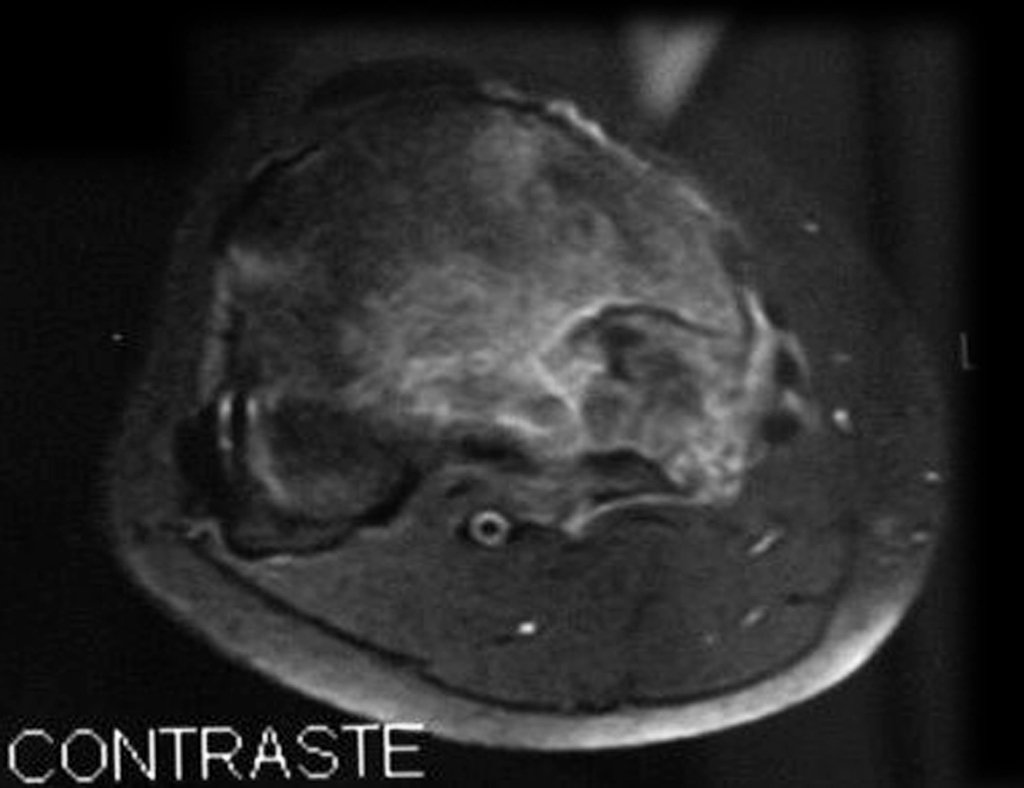
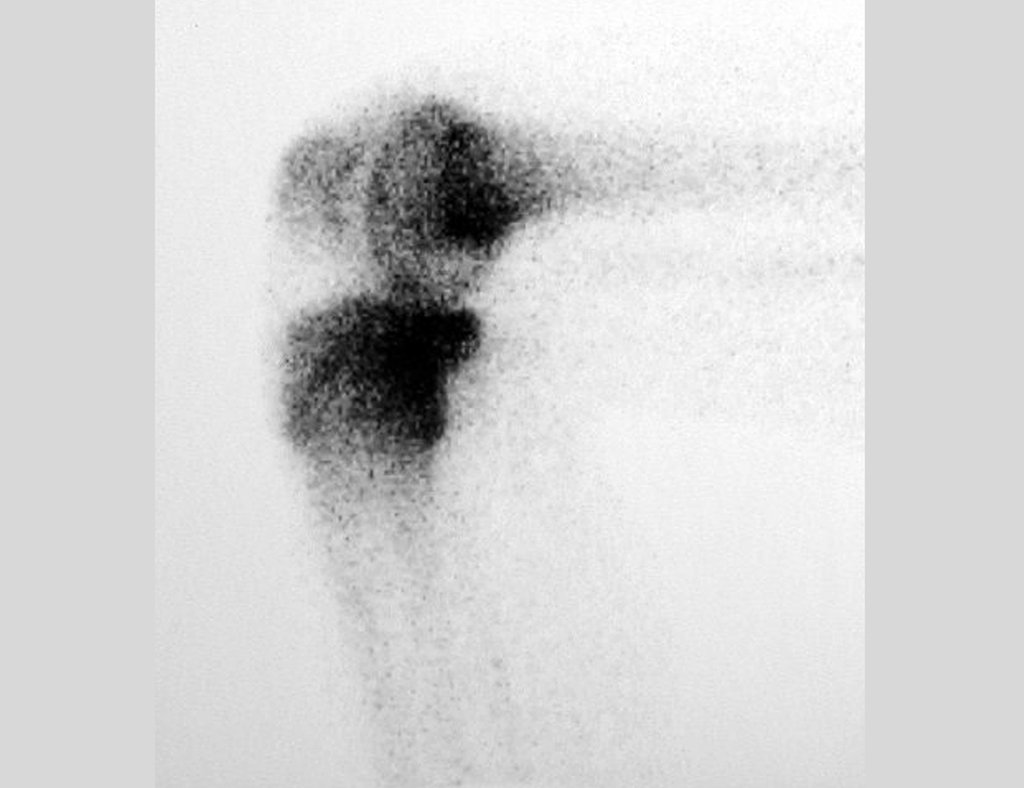
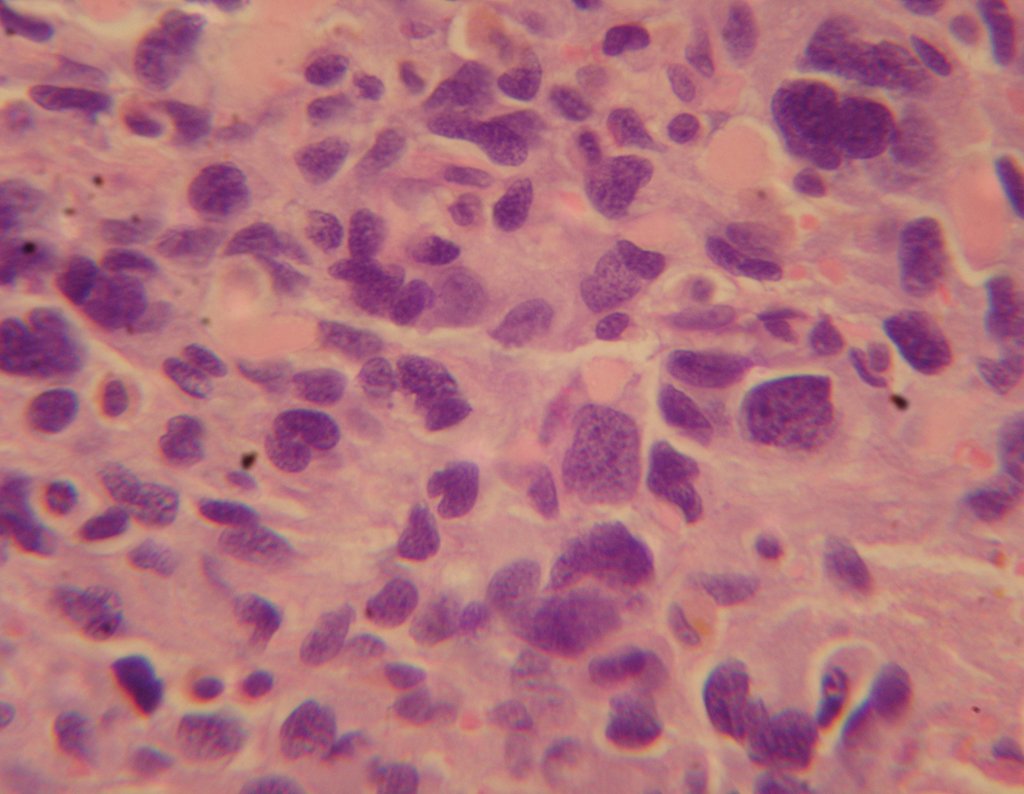
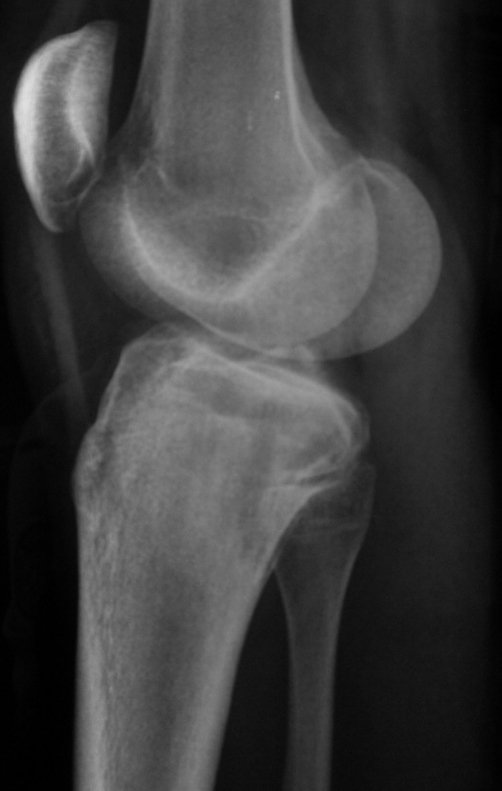
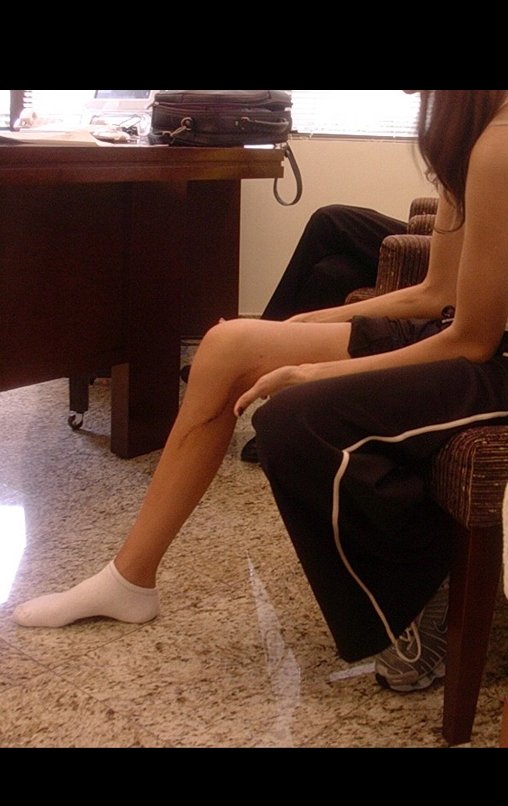
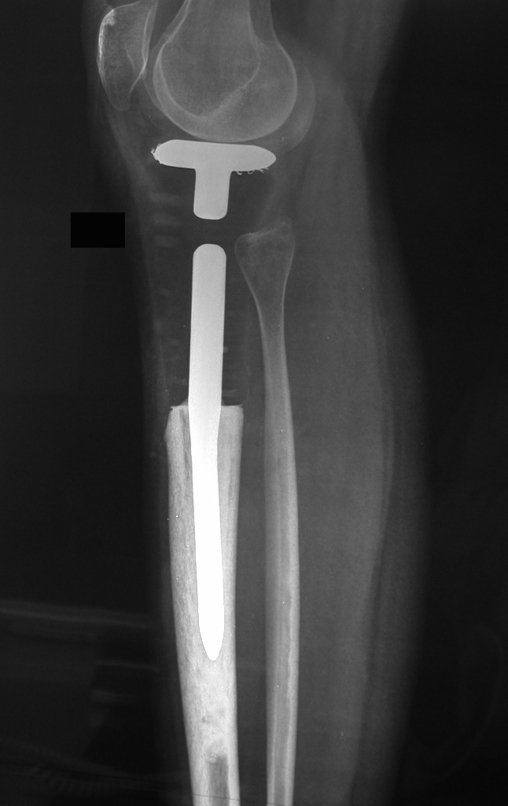
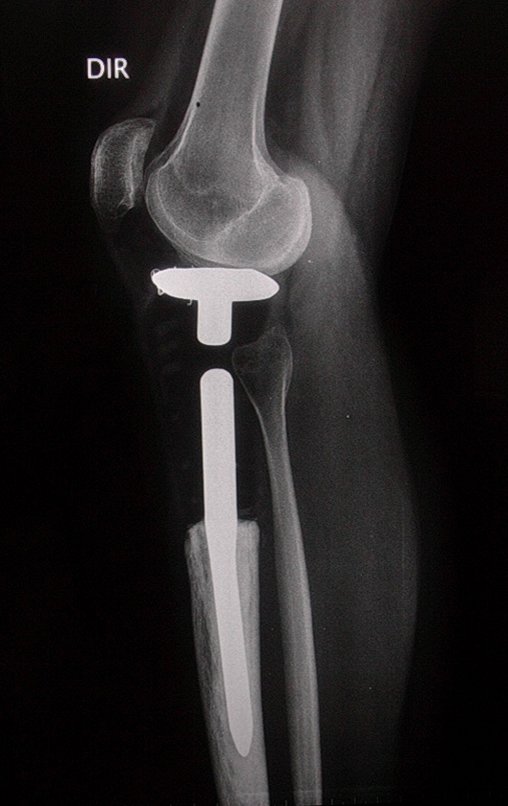
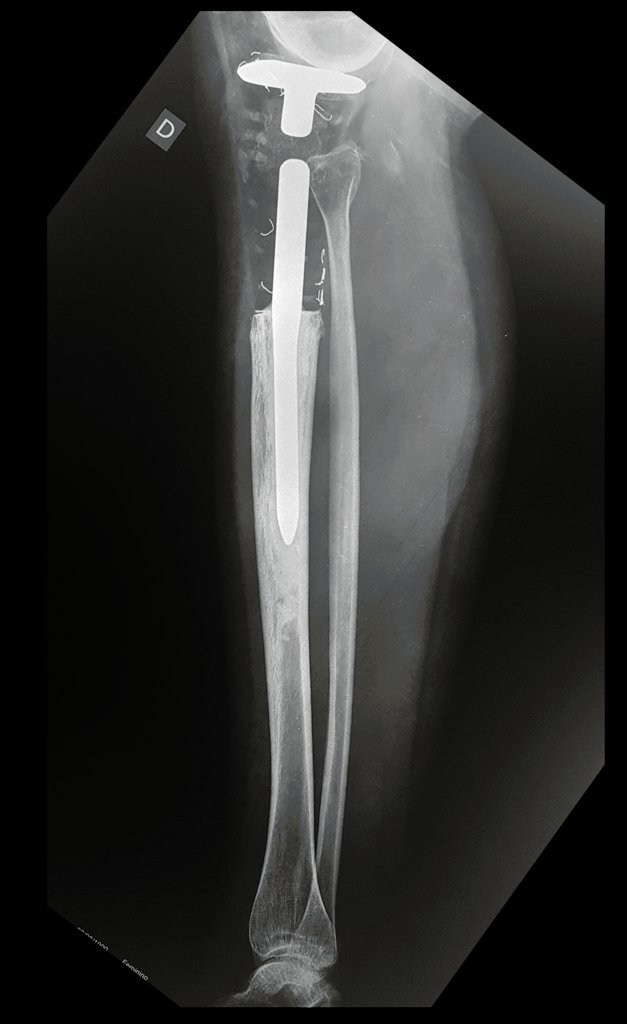
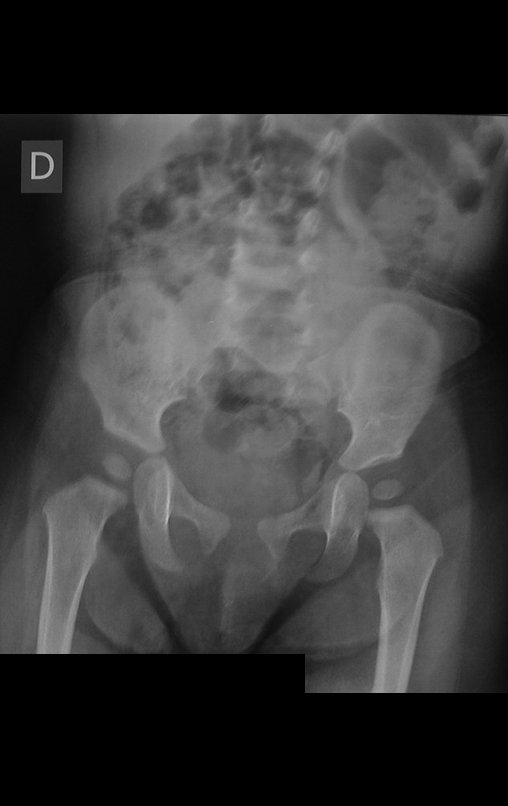
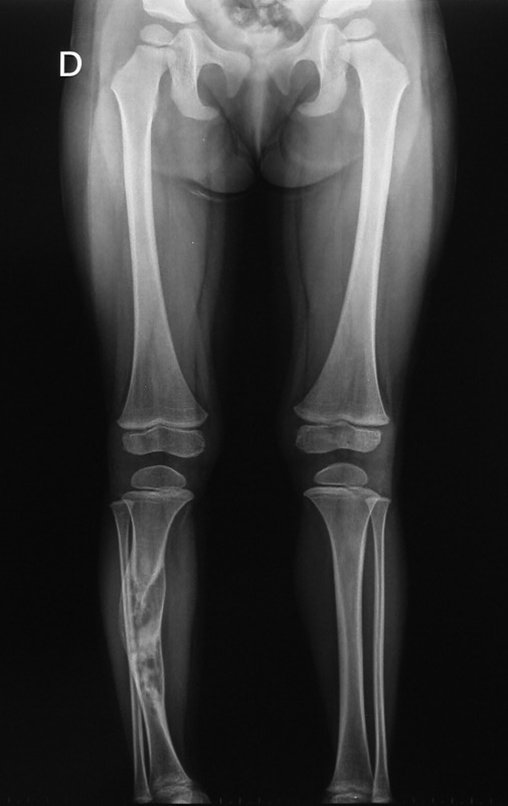
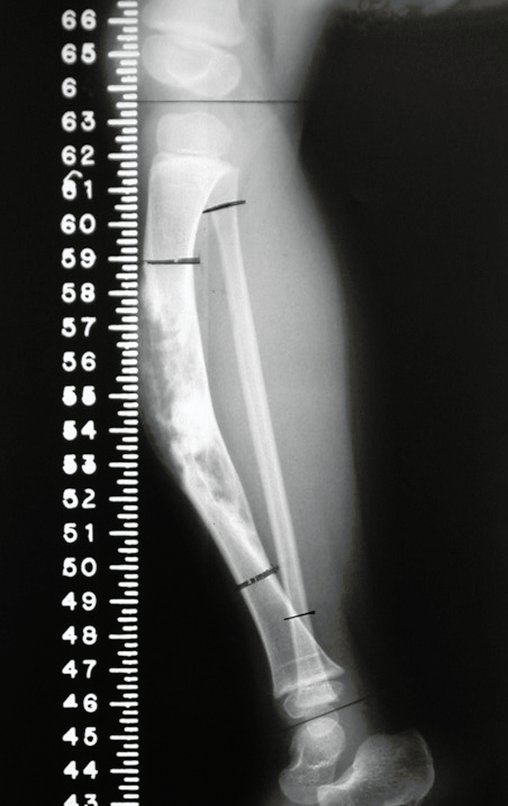
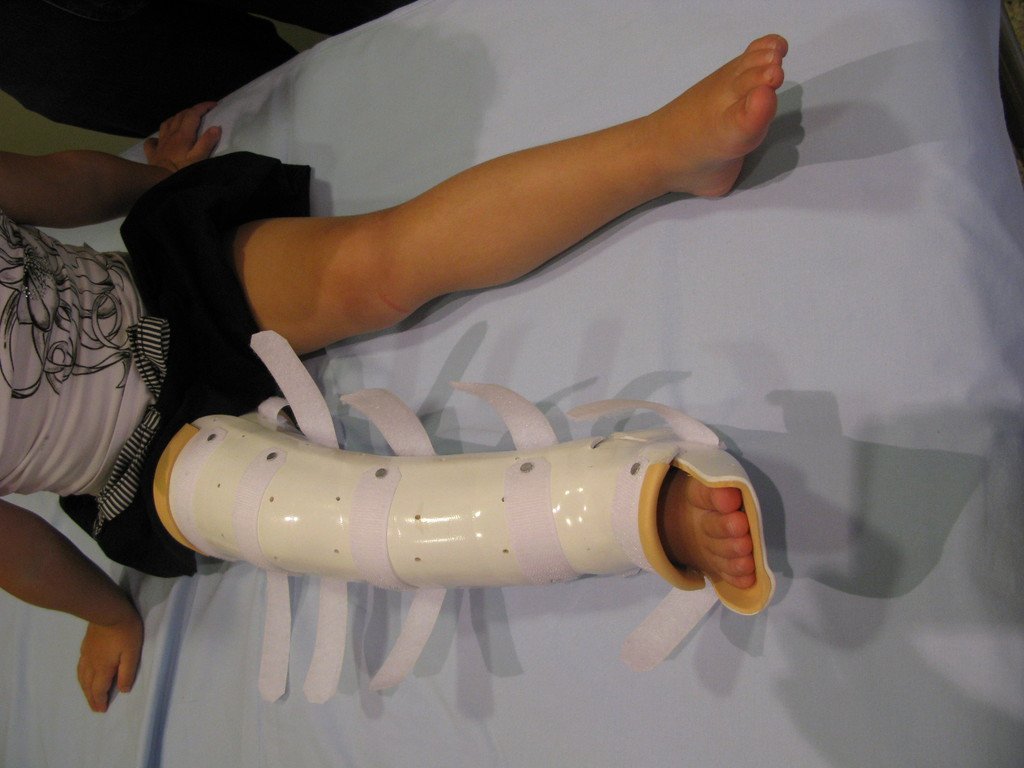
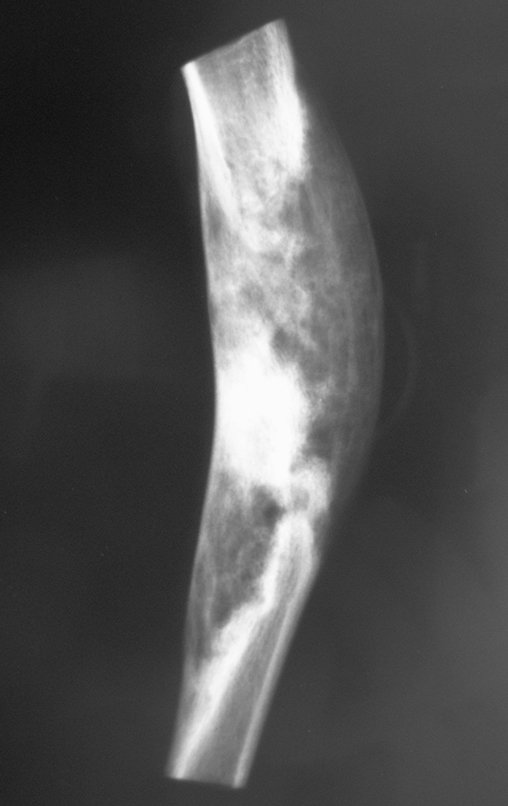
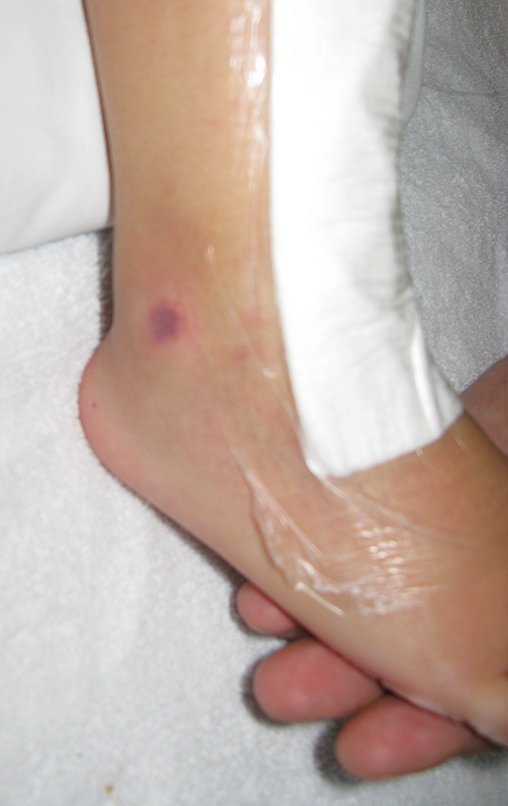
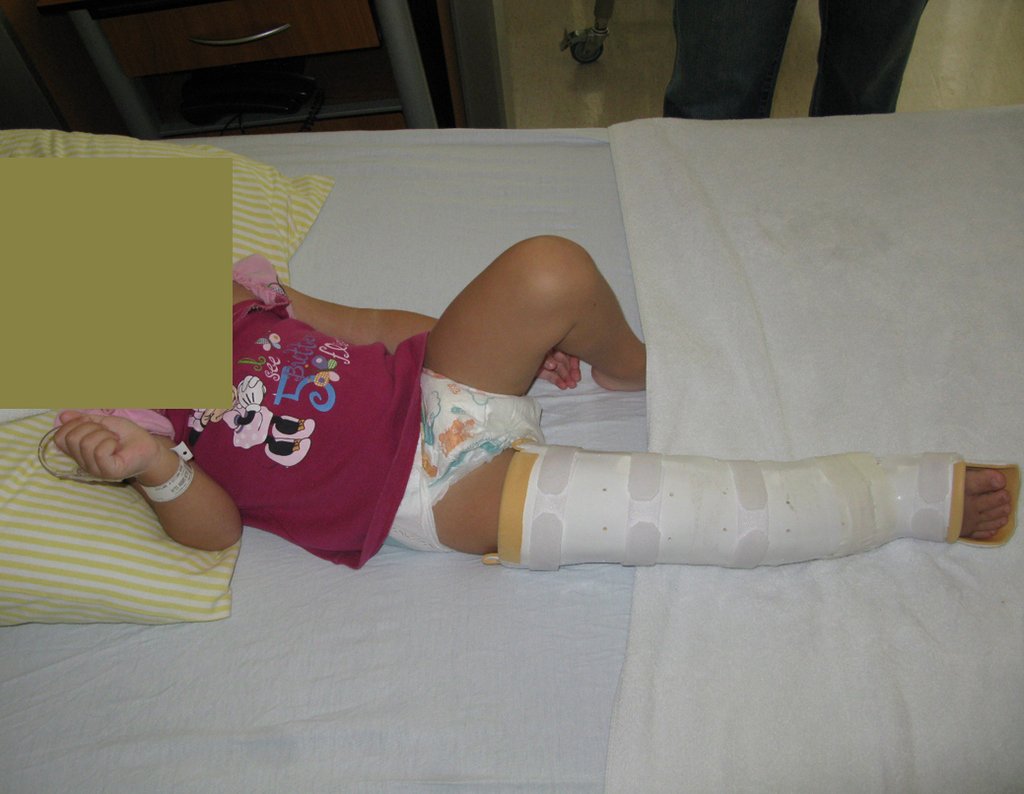
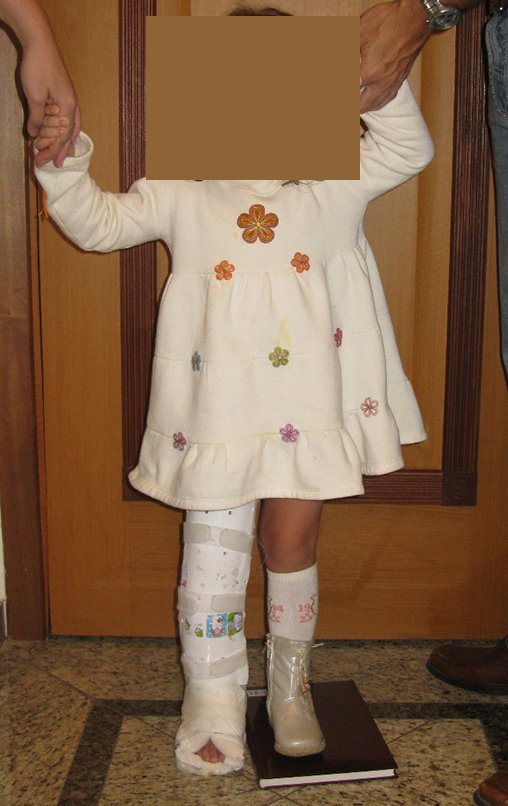
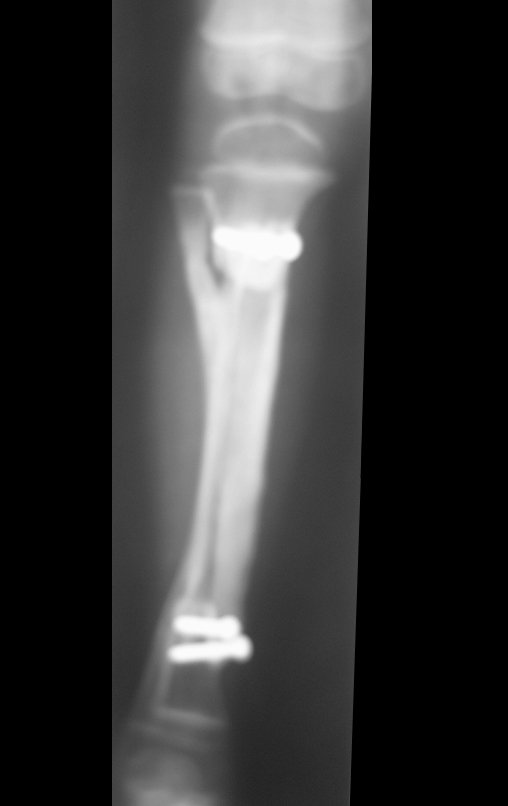
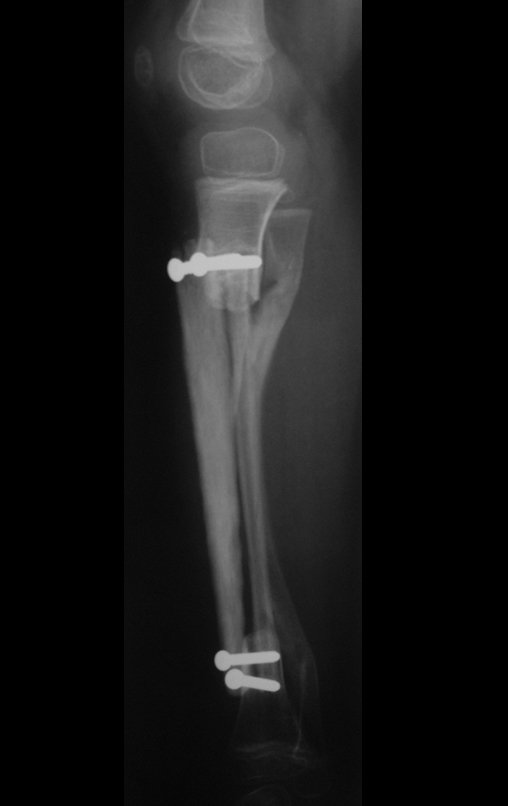
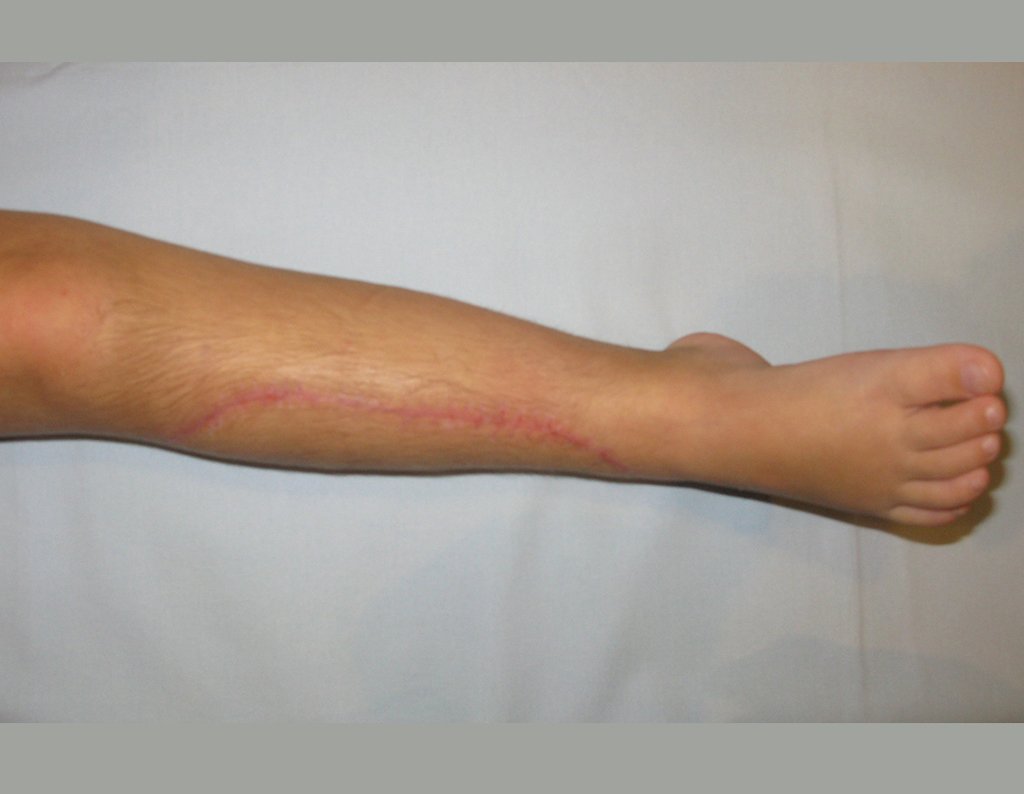
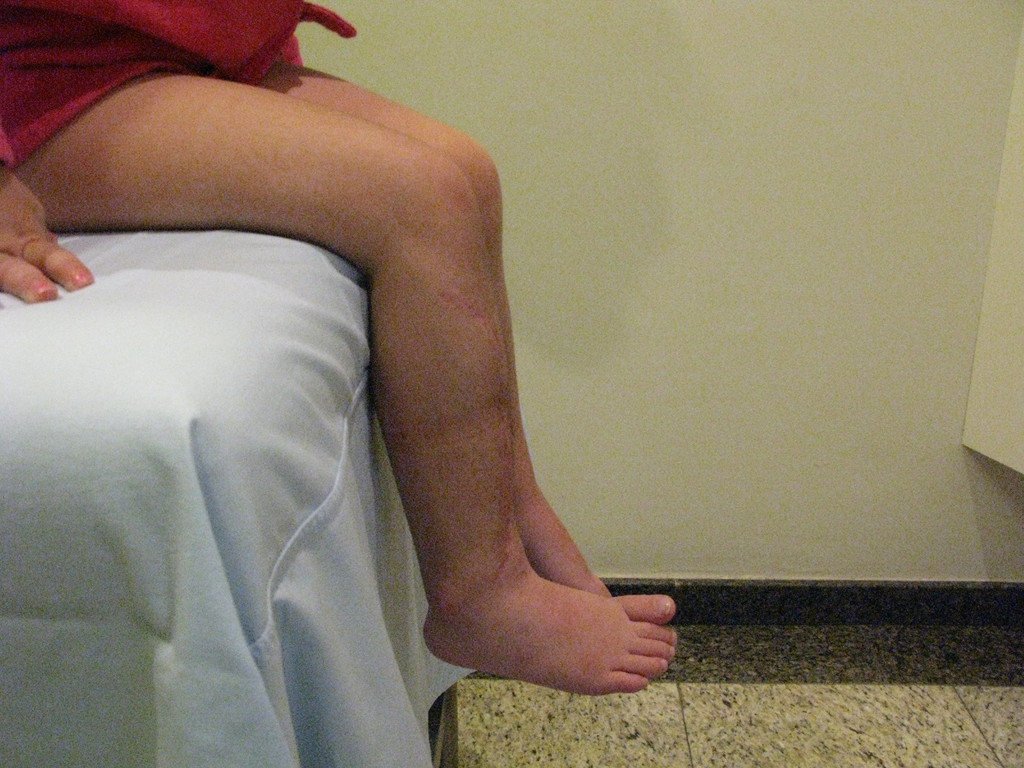
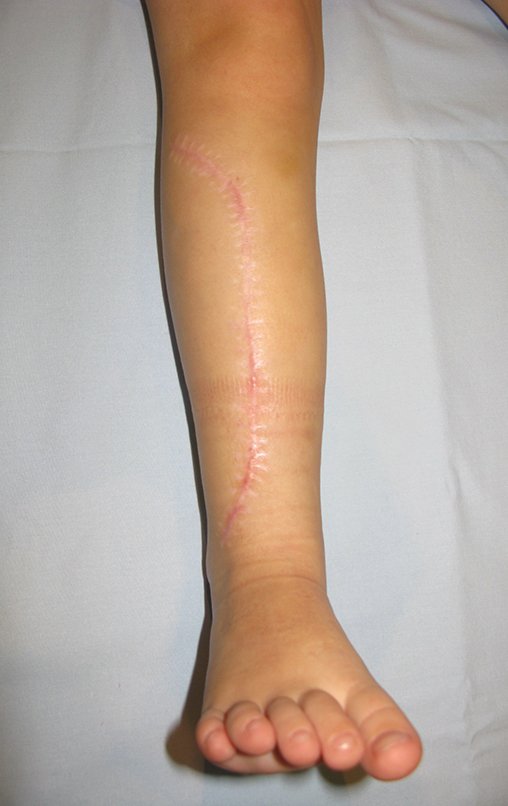
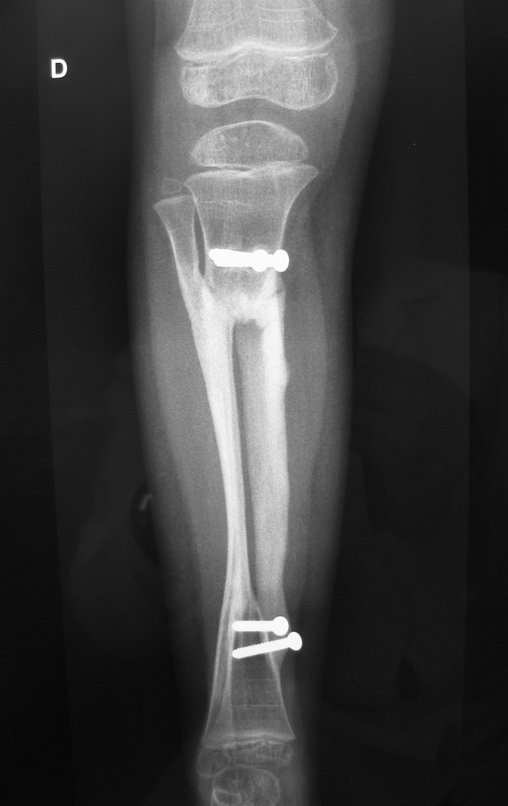
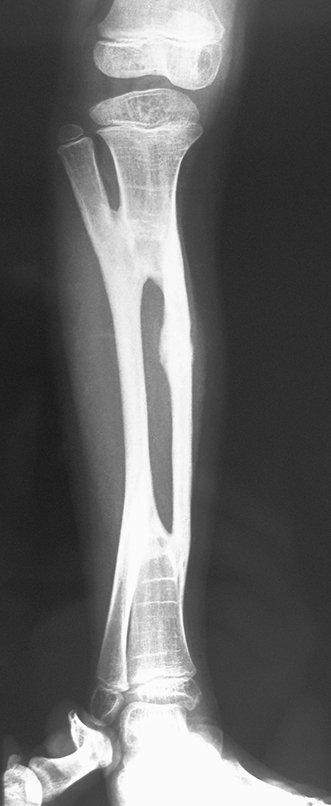
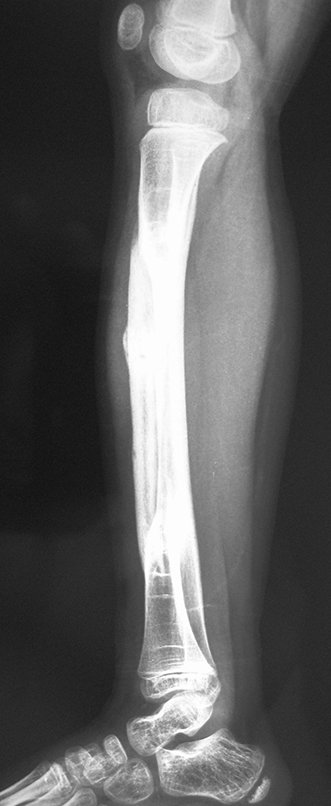
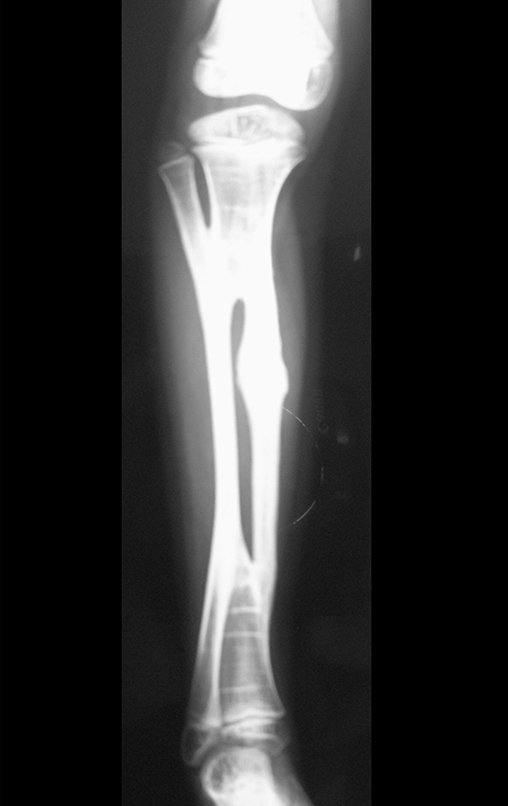
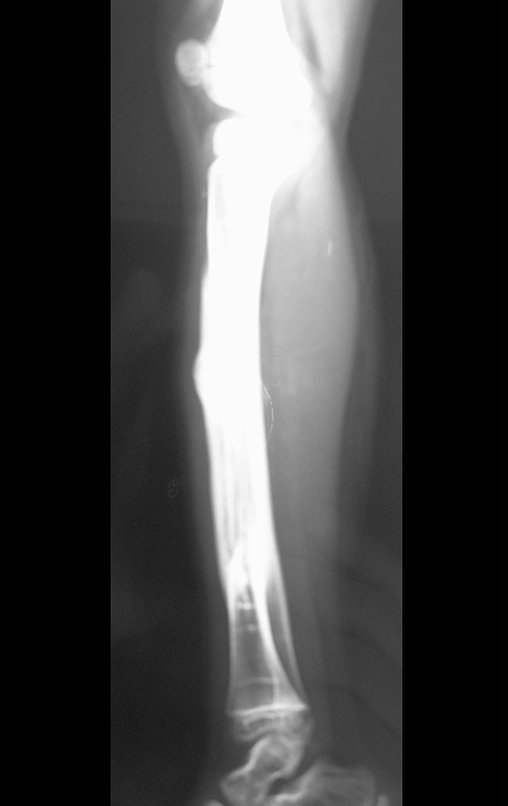
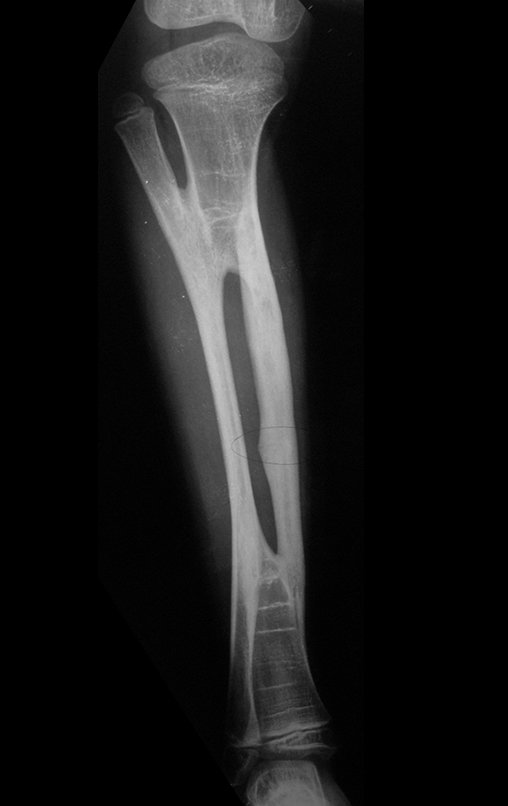
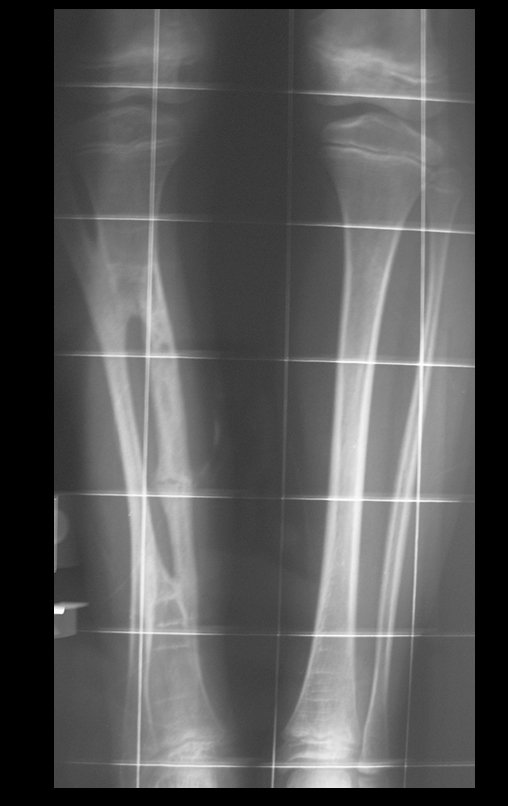
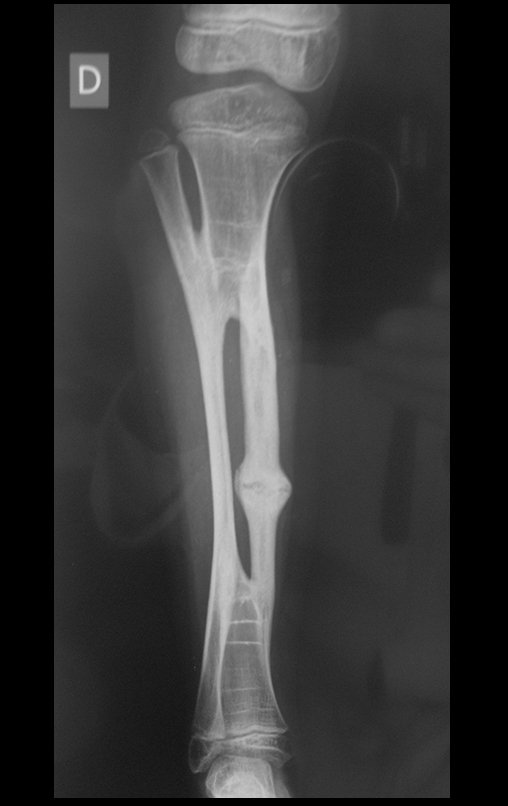
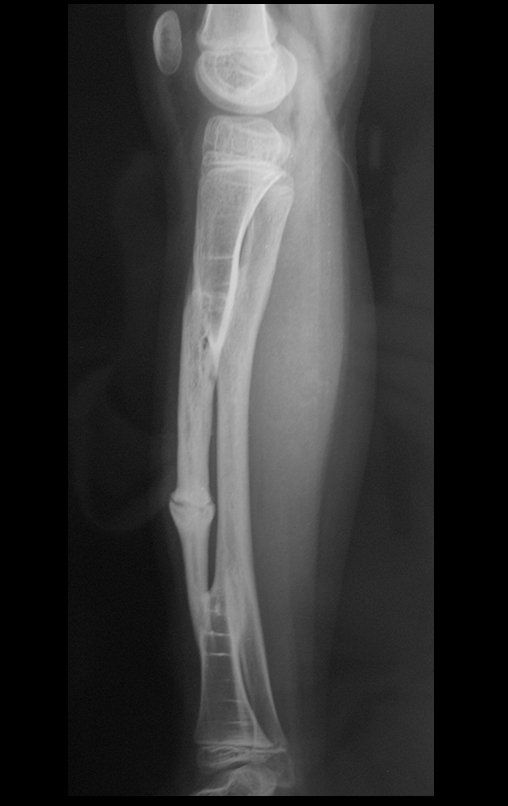
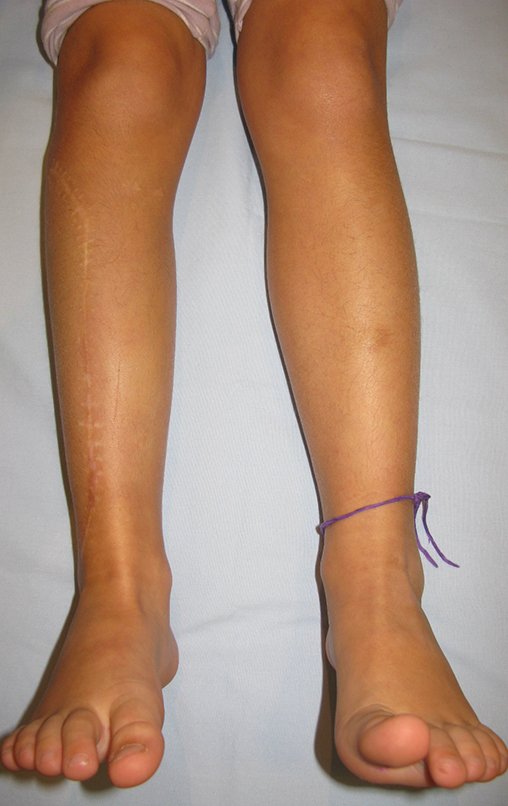
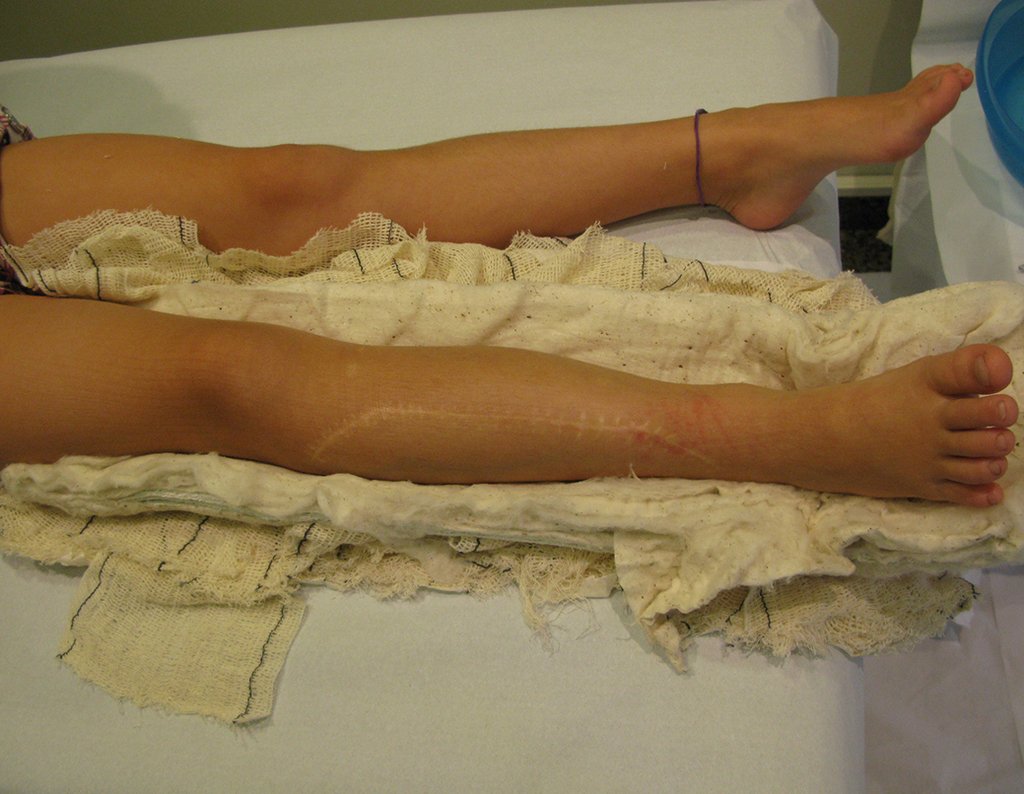
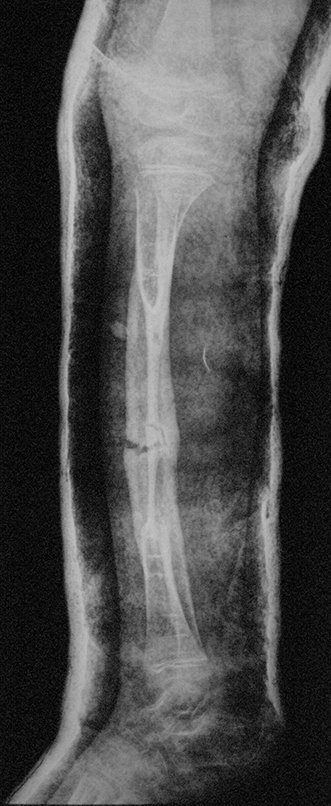
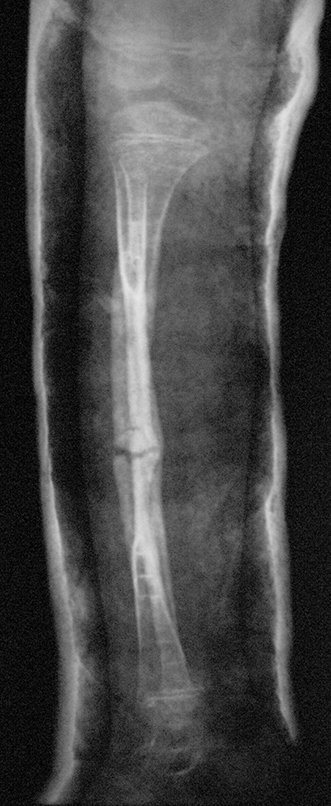
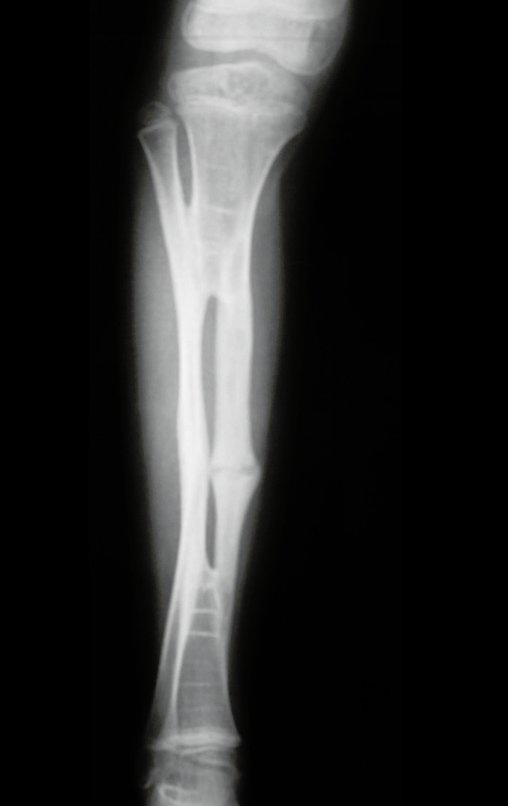
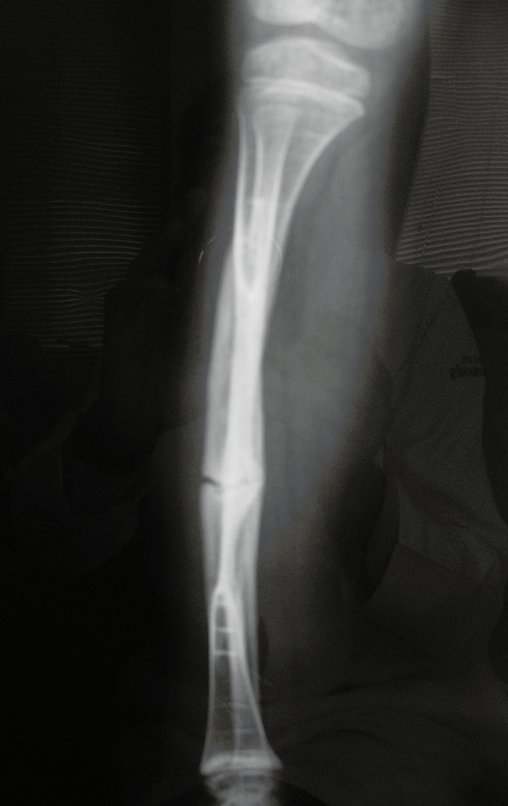
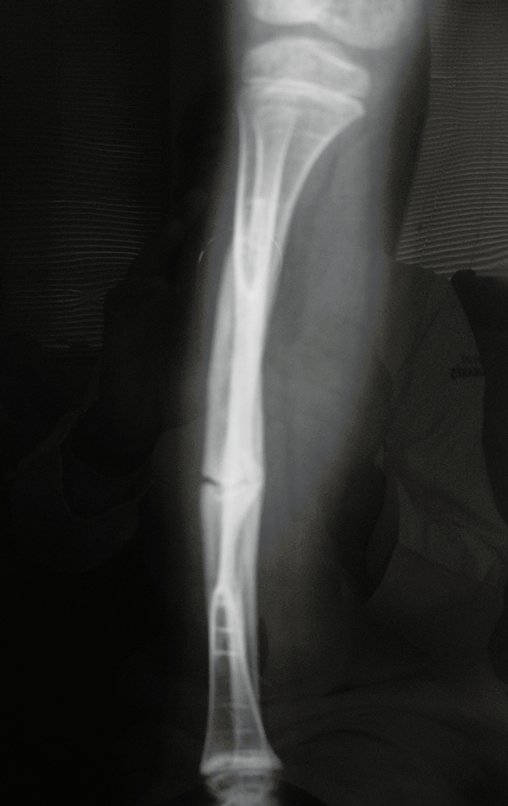
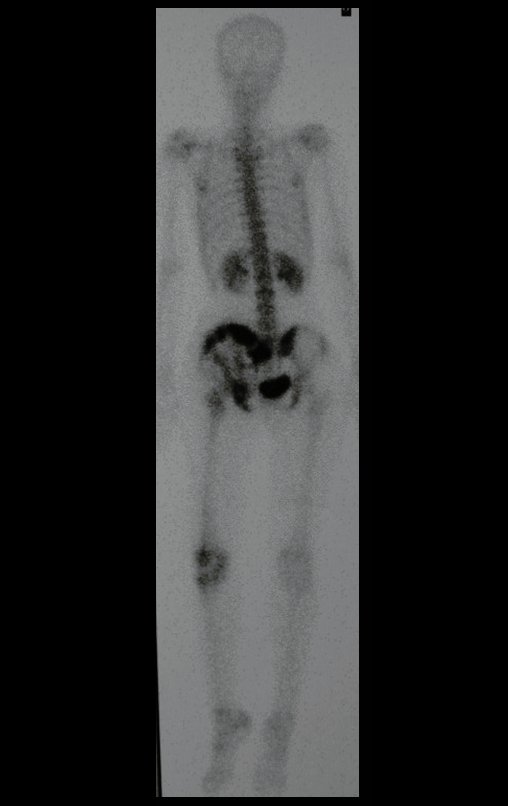
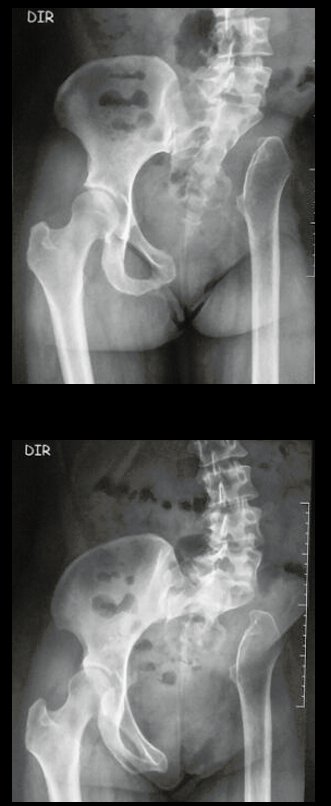
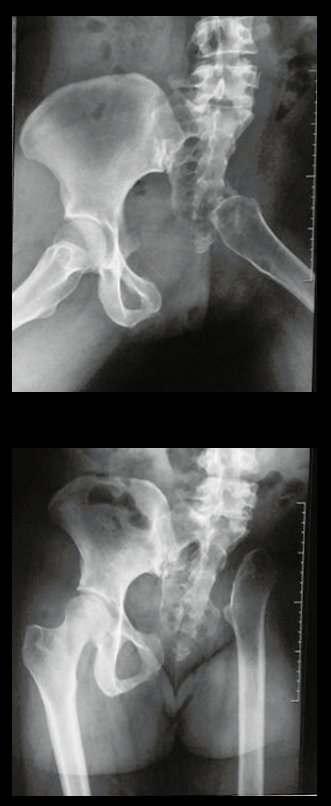
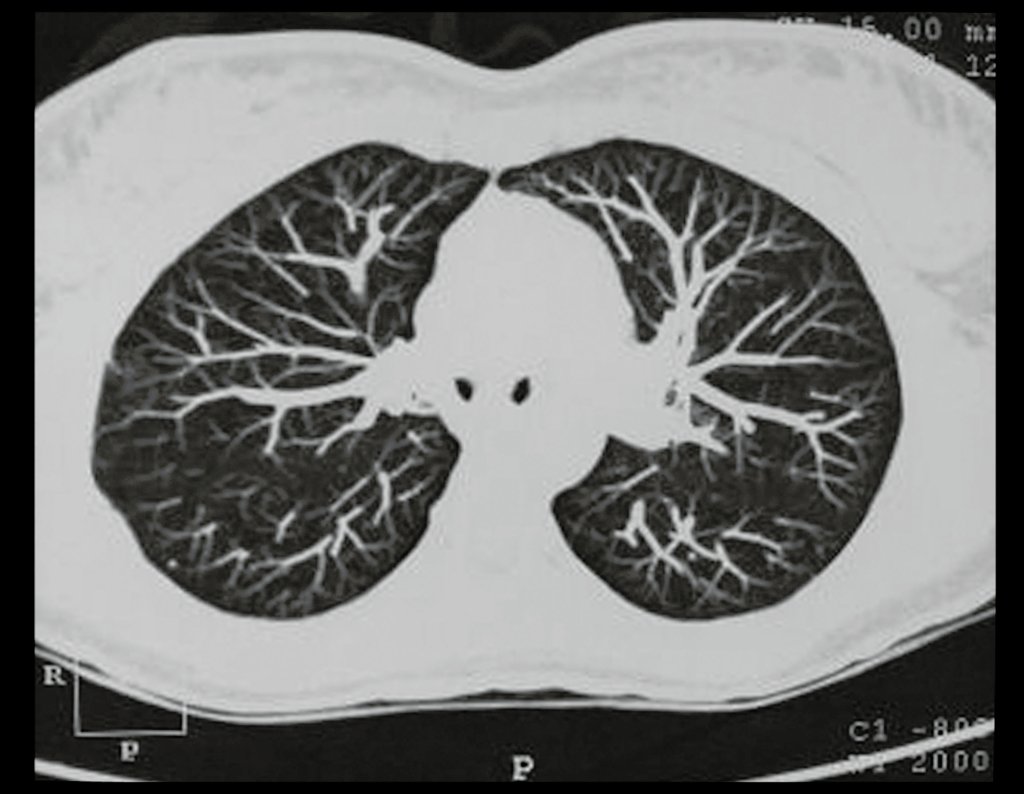
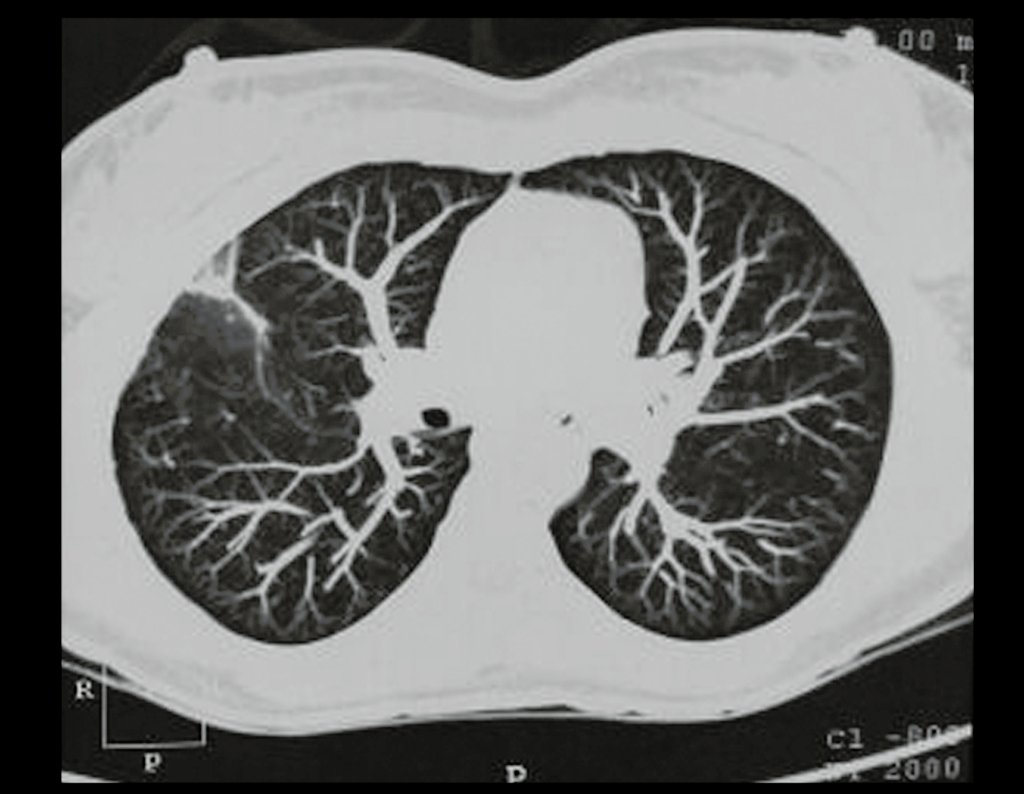
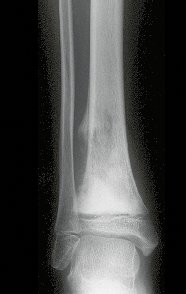
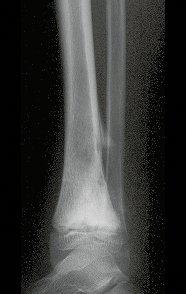
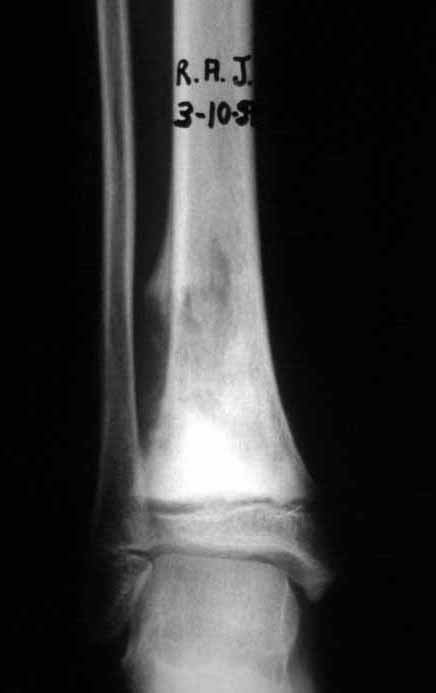
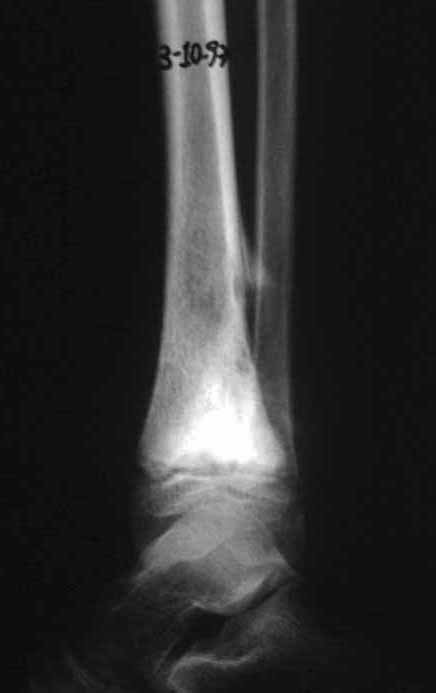
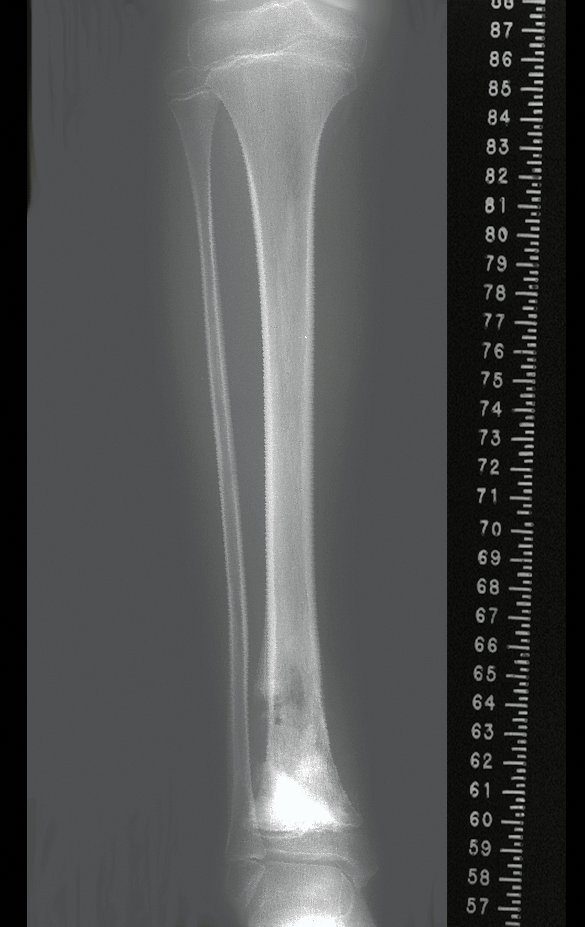
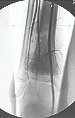
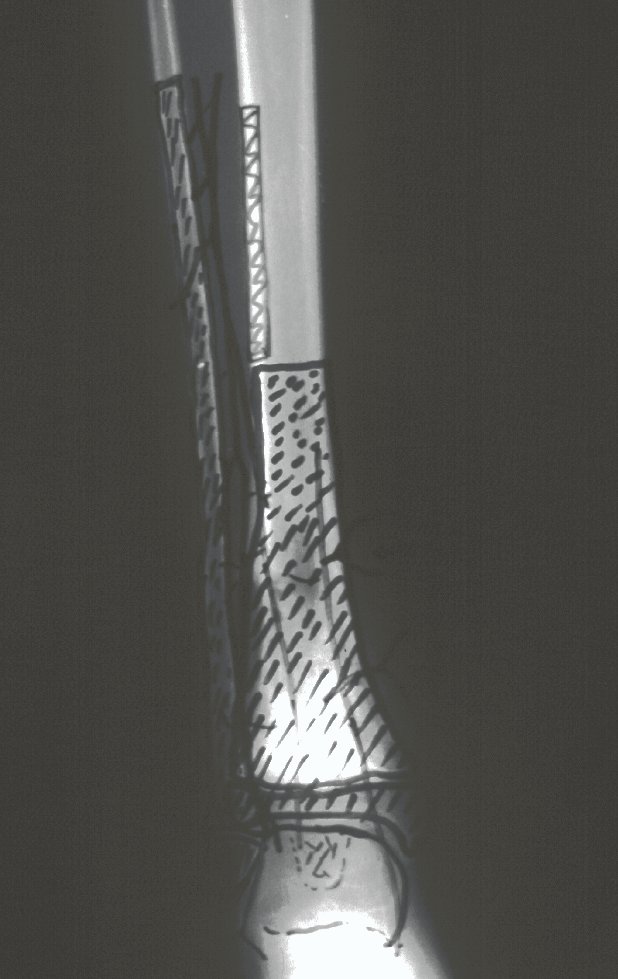
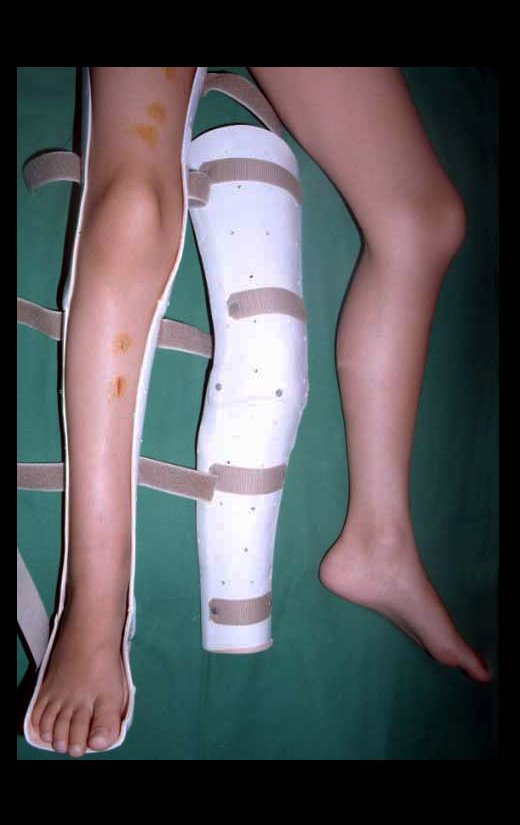
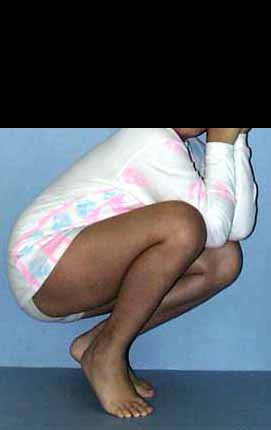
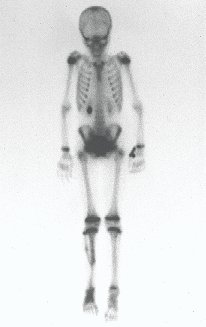
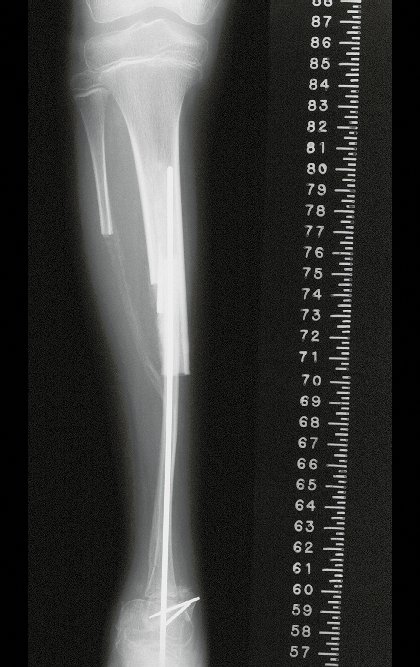
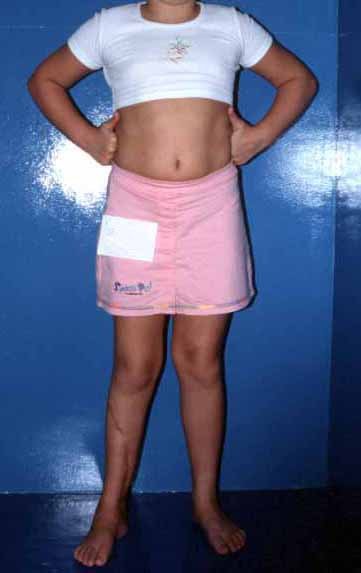
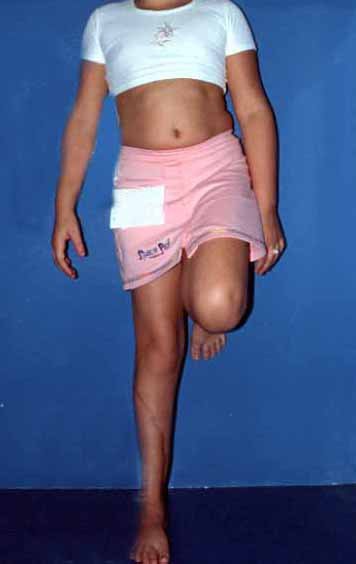
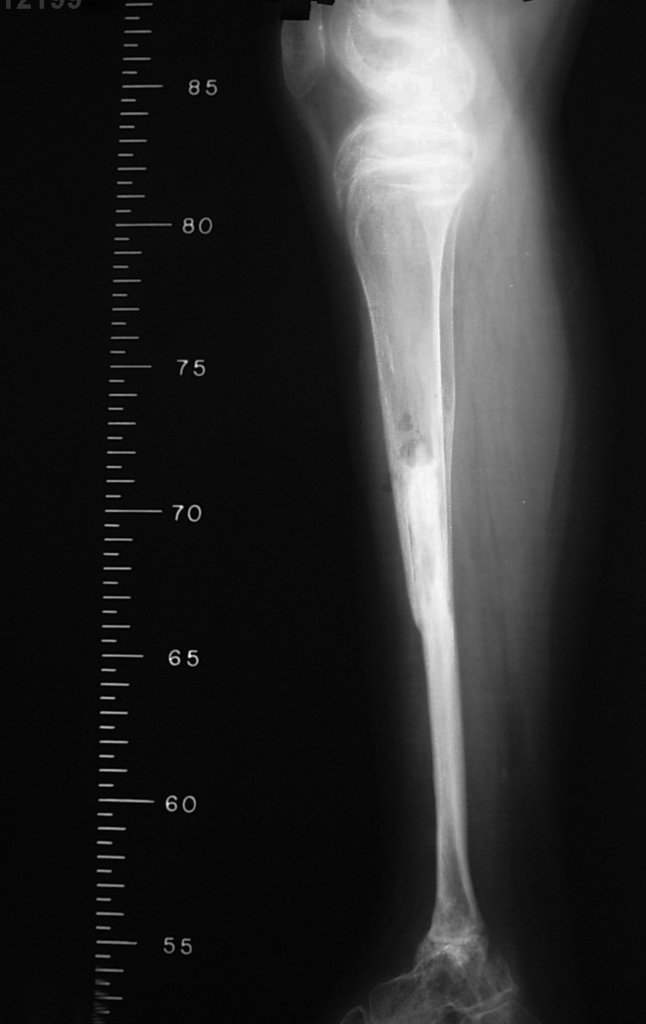
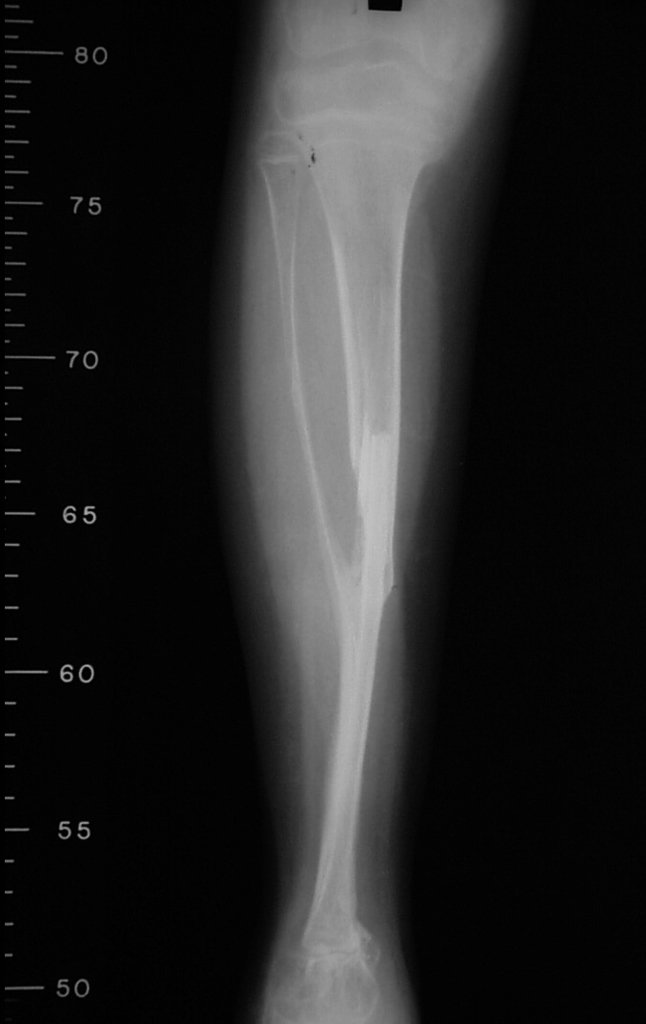
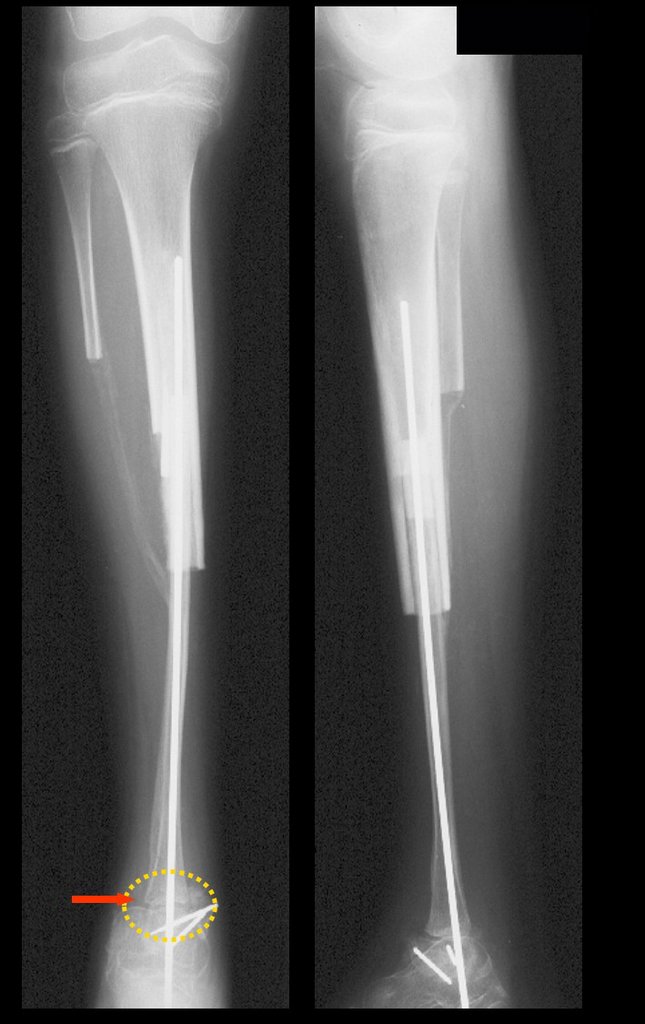
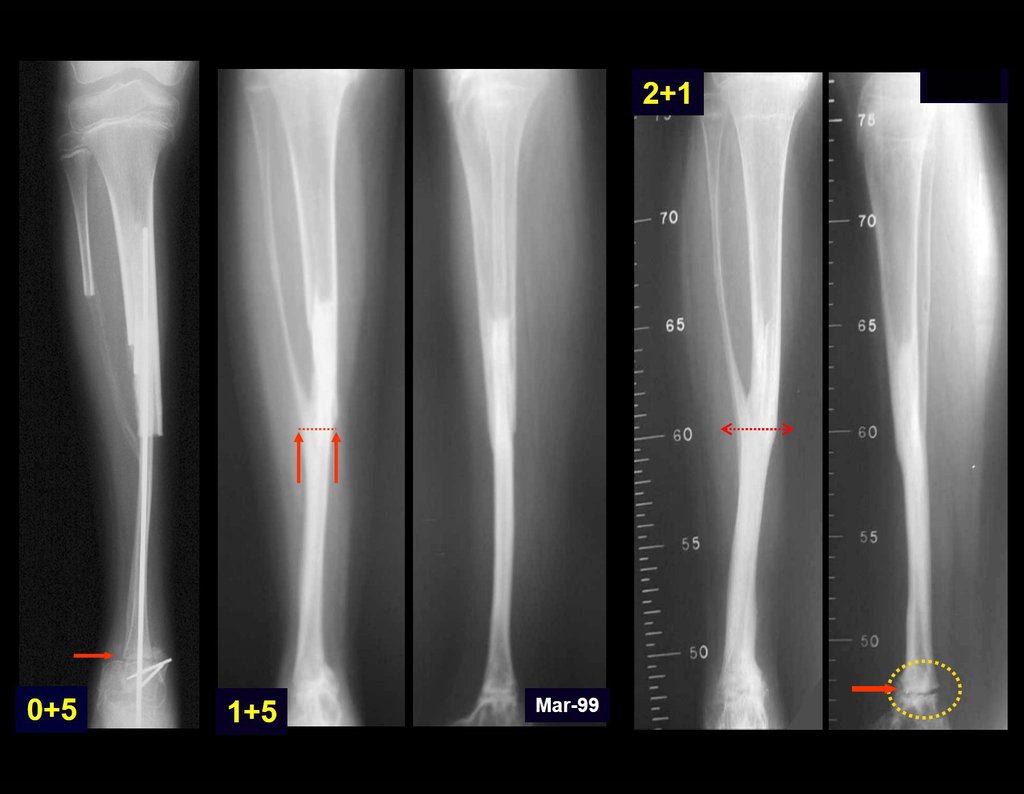
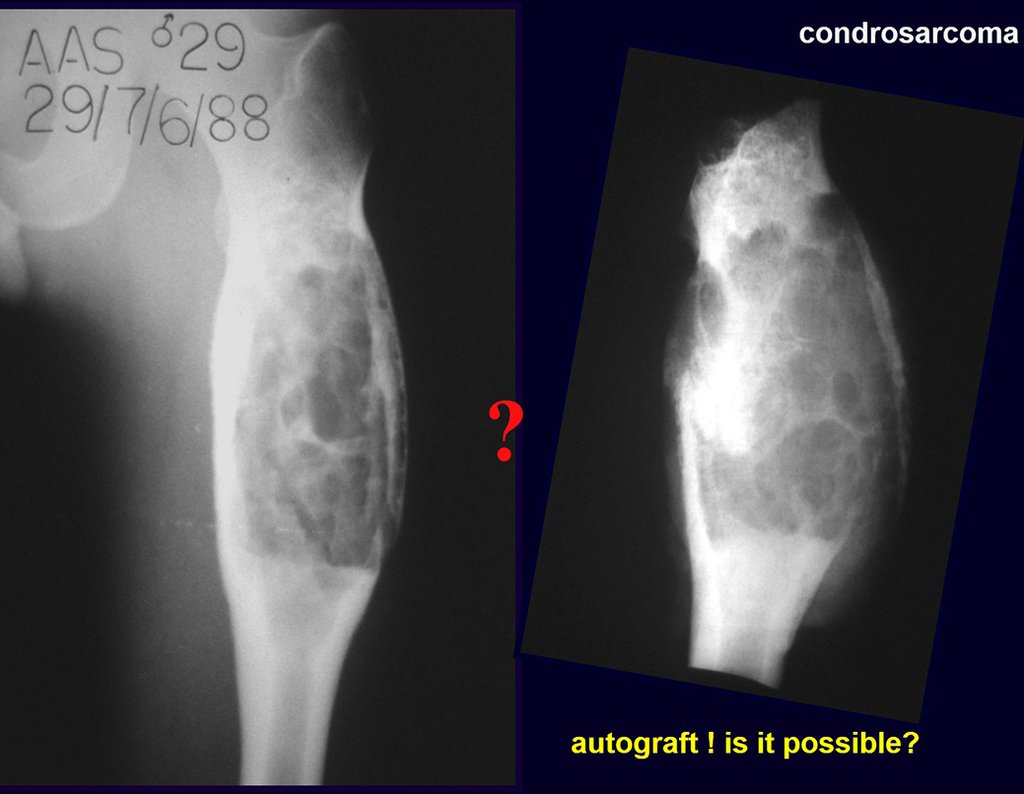
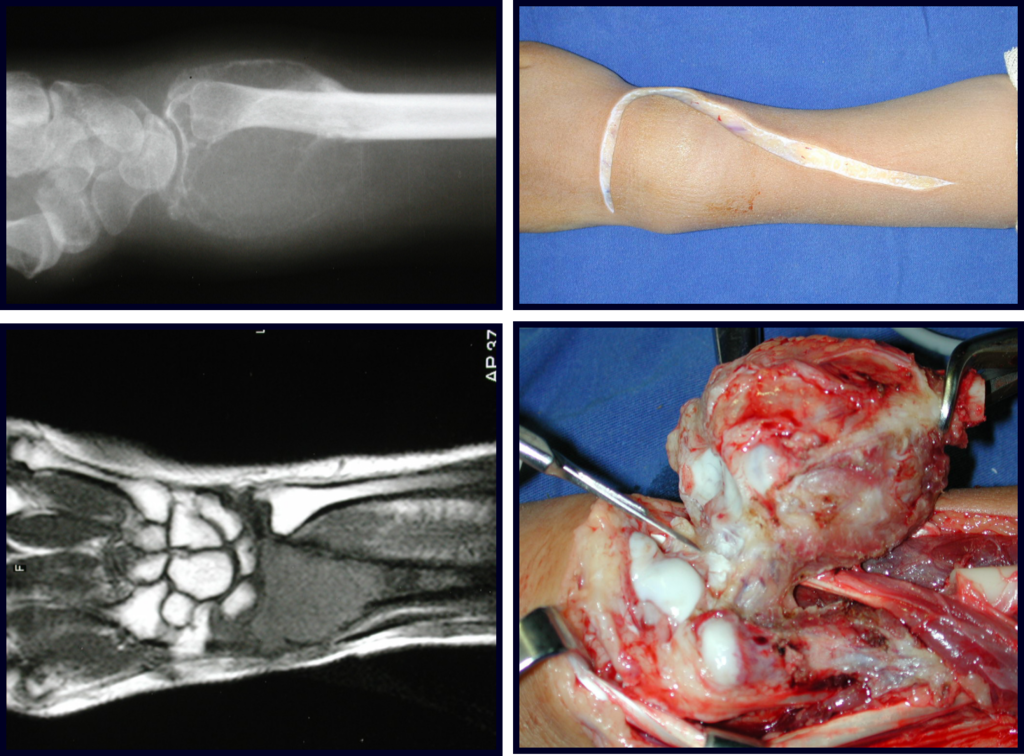
Em maio de 2005, com a suspeita de tumor de células gigantes, foi encaminhada para um segundo hospital, cinco meses do primeiro atendimento. Novo encaminhamento foi feito, agora para nosso atendimento, em outubro daquele ano (Figuras 7 à 10).
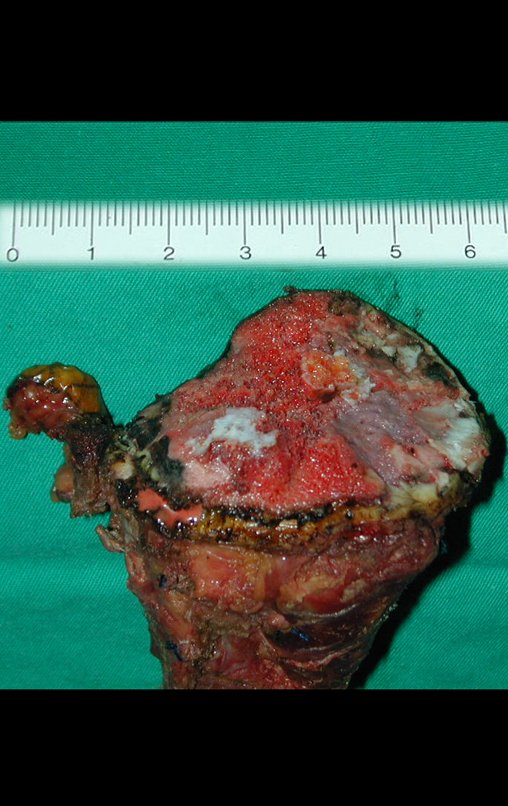
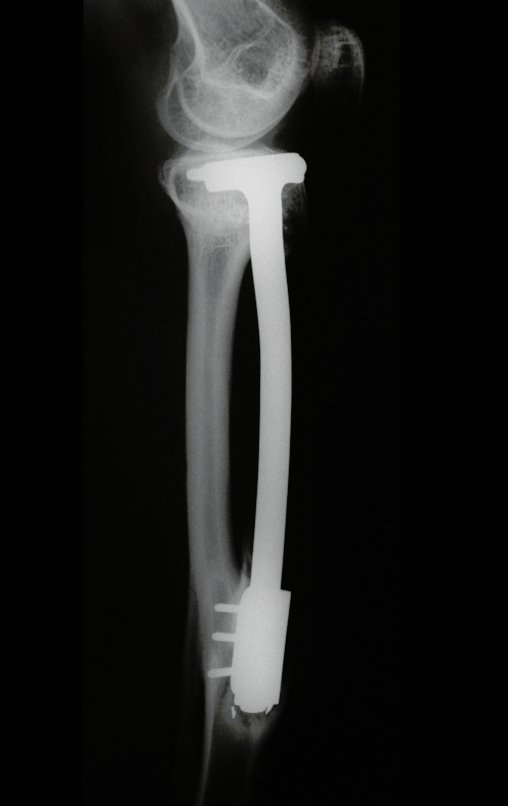
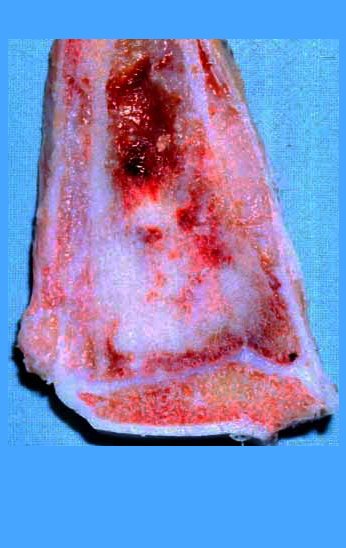
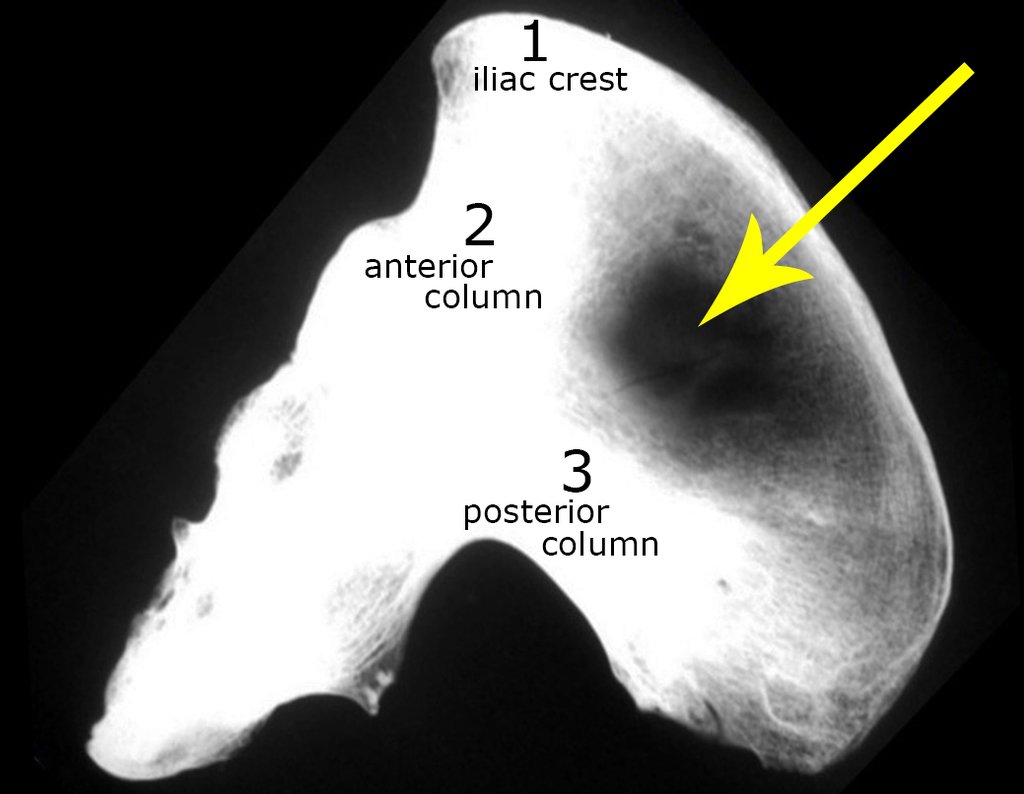
Com este estudo, confirmamos a agressividade local do tumor, e a grande destruição da extremidade distal do rádio esquerdo, com fratura por infracção, deformidade articular e encurtamento do rádio. Nesta situação o tratamento intralesional deve ser contraindicado, devido à alta possibilidade de recidiva local, além da perda da função. Oncologicamente está indicada a ressecção segmentar do rádio, e reconstrução do punho. A artrodese pode ser uma alternativa, mas preferimos preservar a função e a anatomia do punho, sempre que possível. Neste caso, optamos por reconstruir com enxerto autólogo não vascularizado, obtido do segmento proximal da fíbula ipsilateral, que mimetiza melhor o rádio.
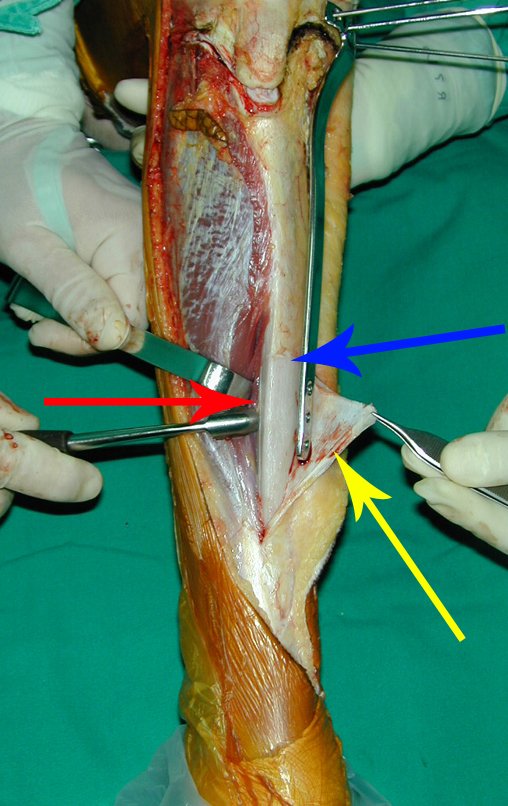
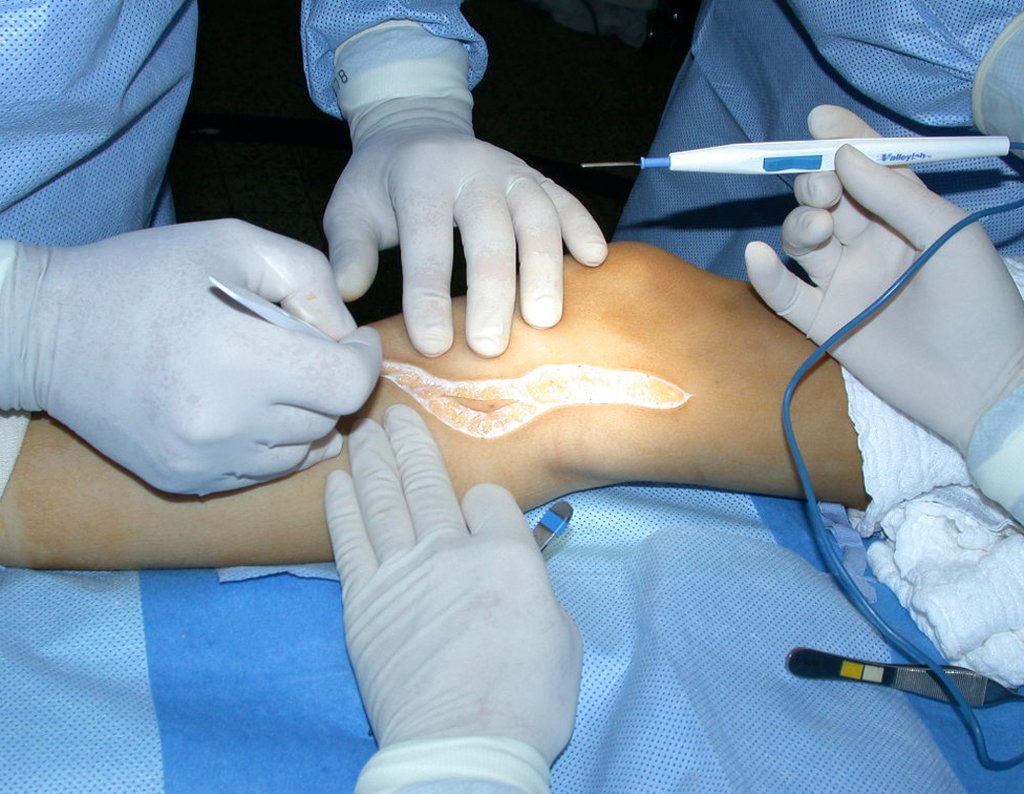
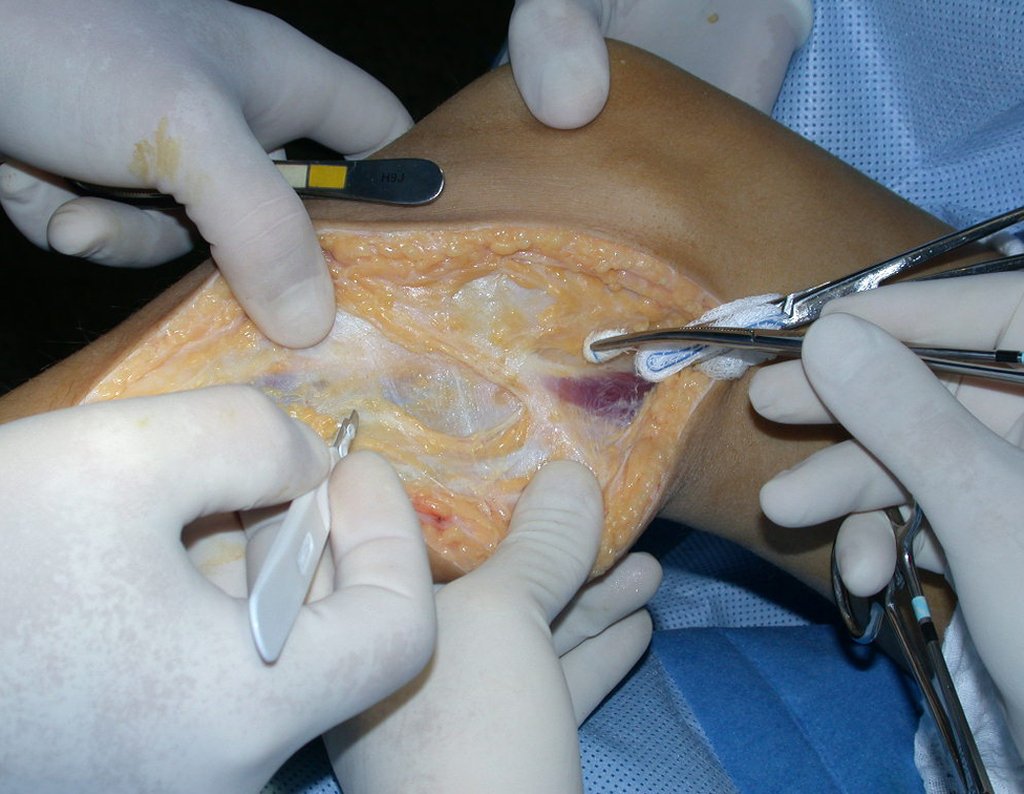
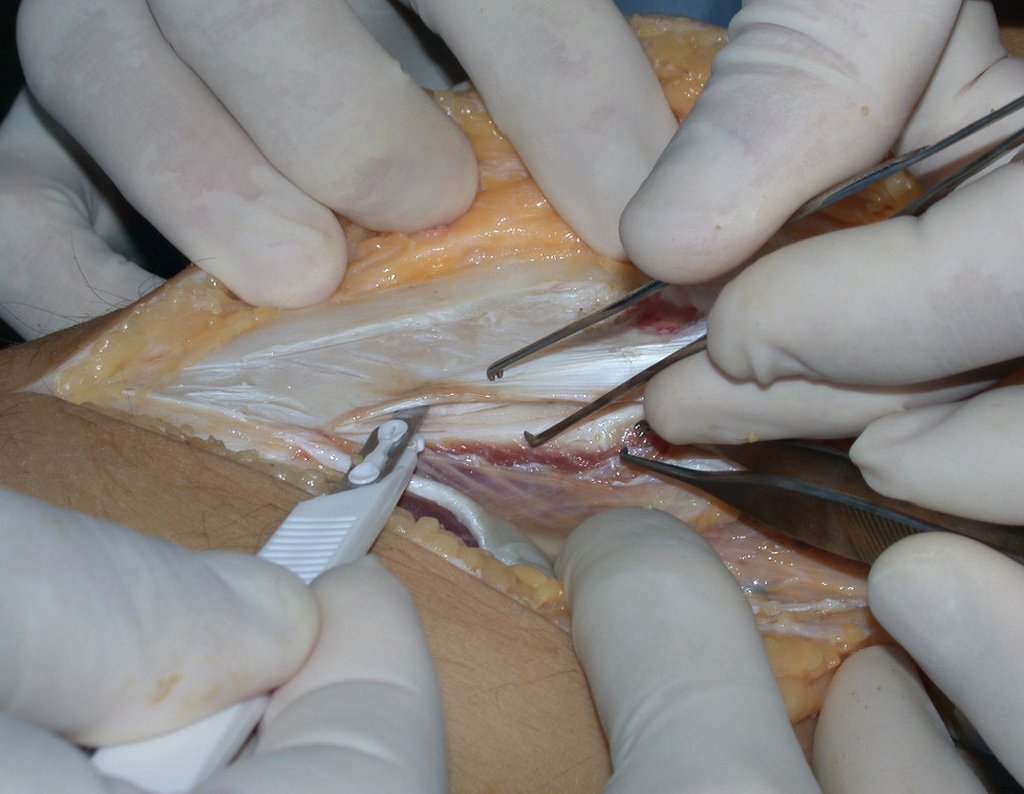
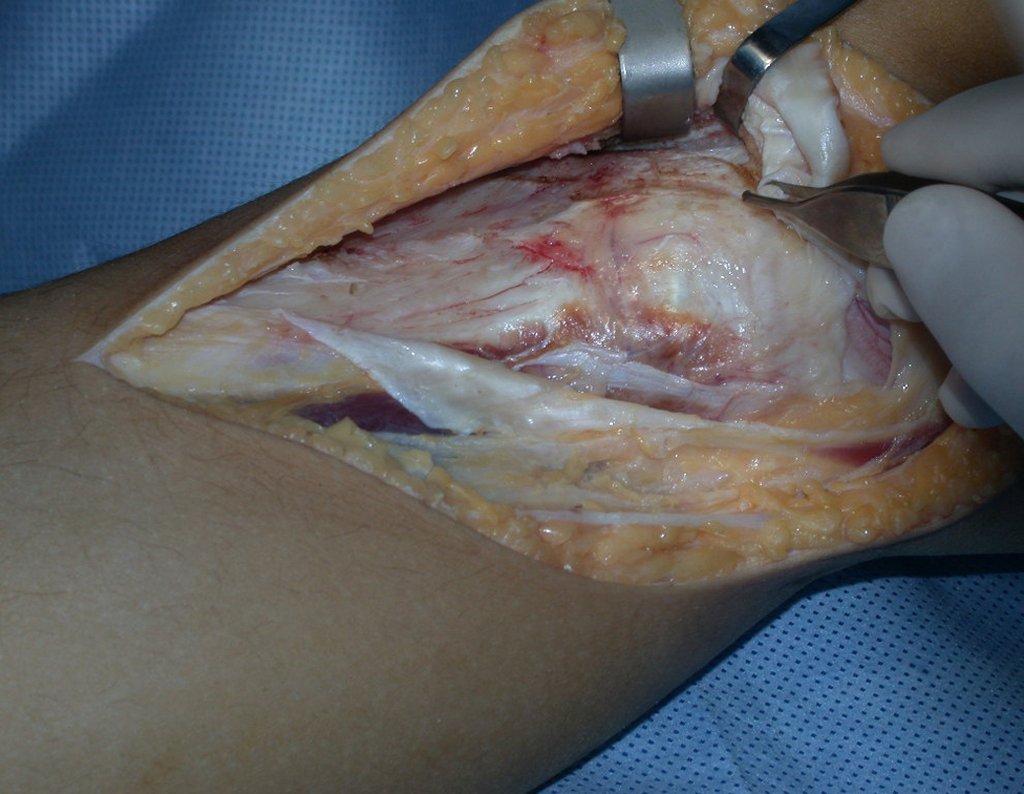
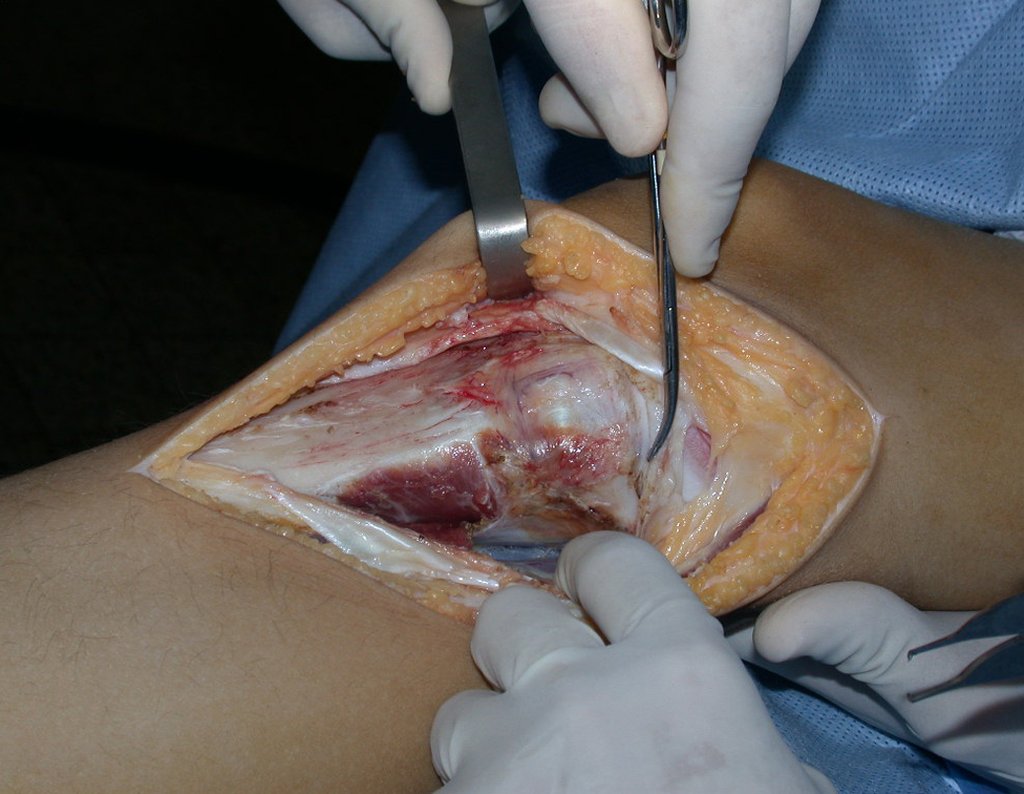
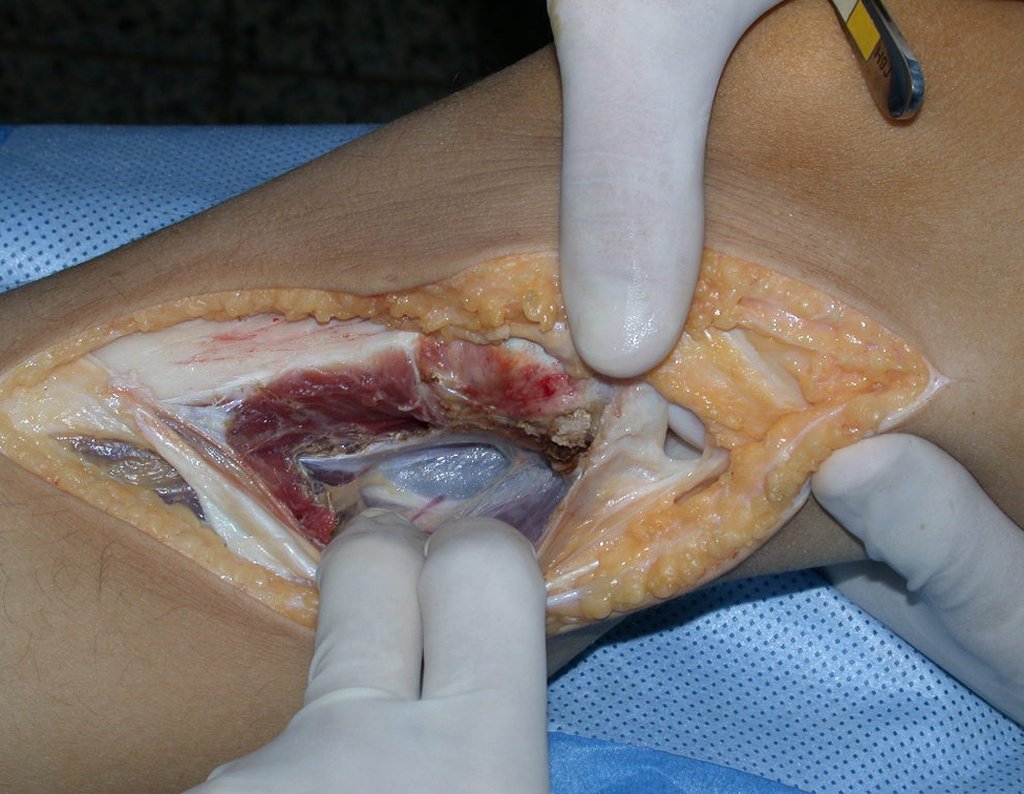
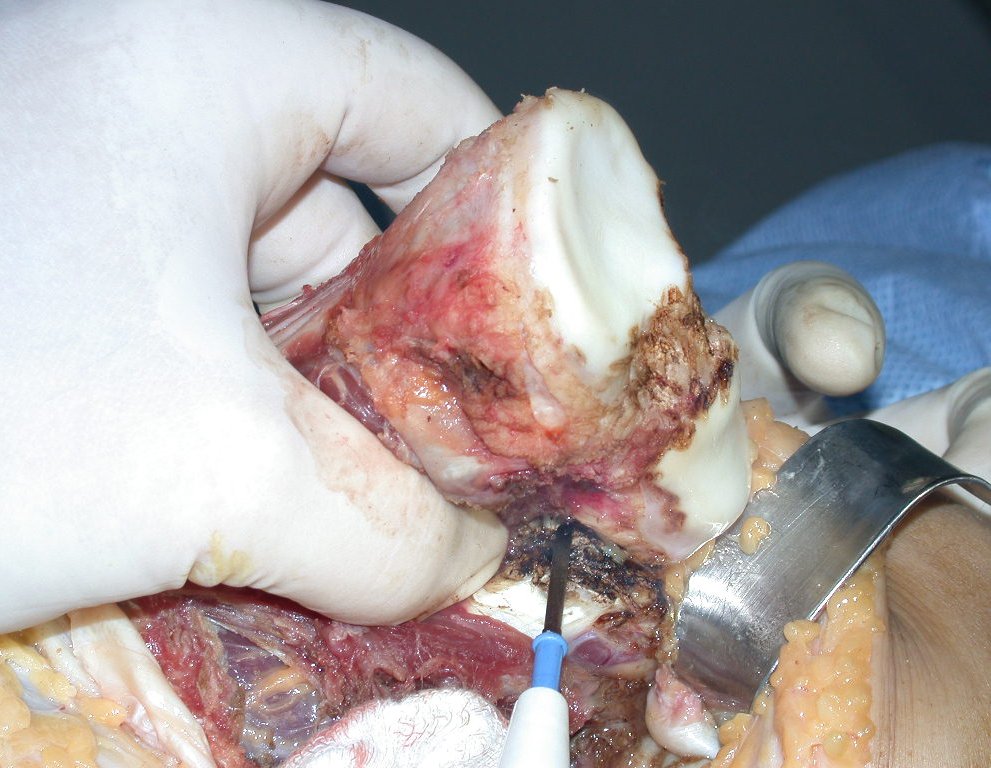
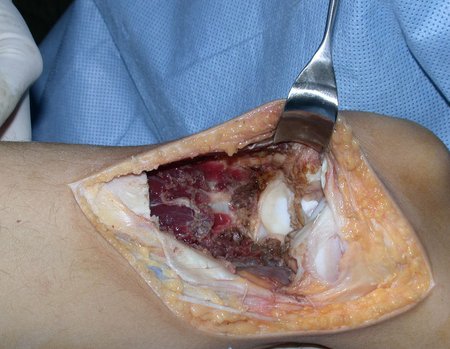
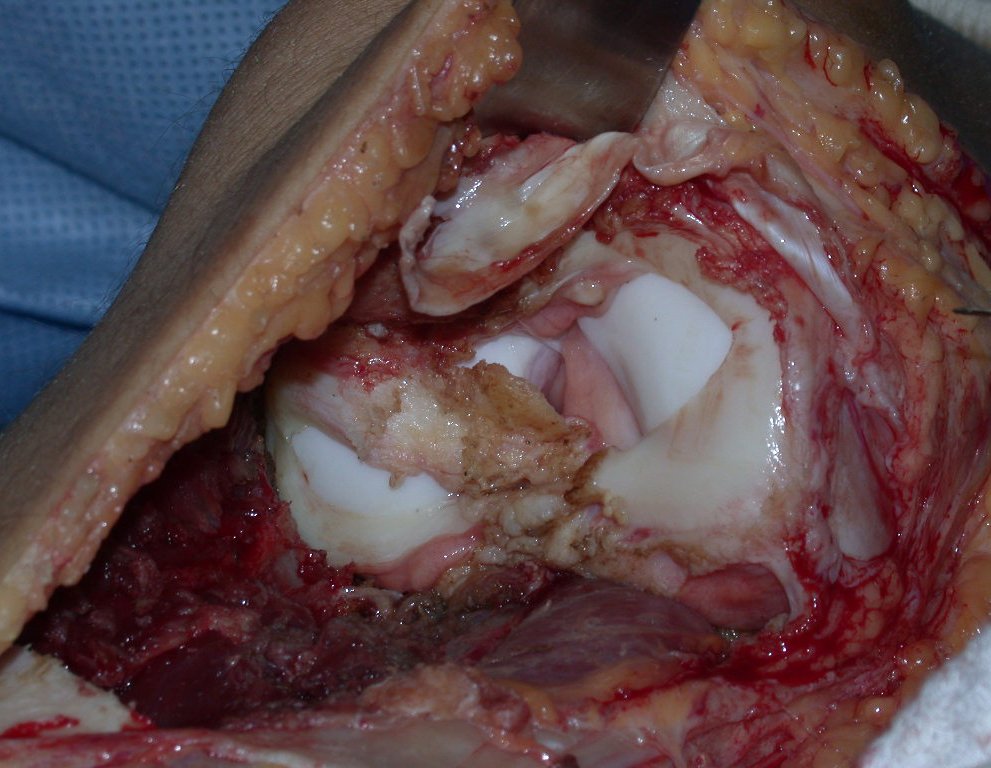
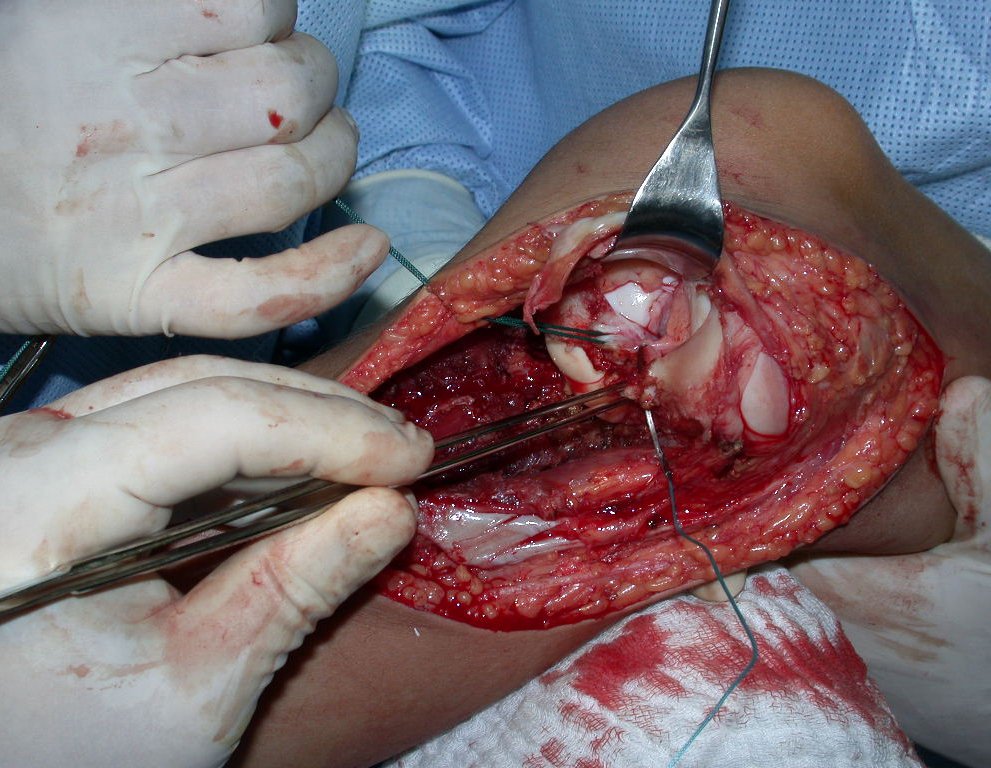
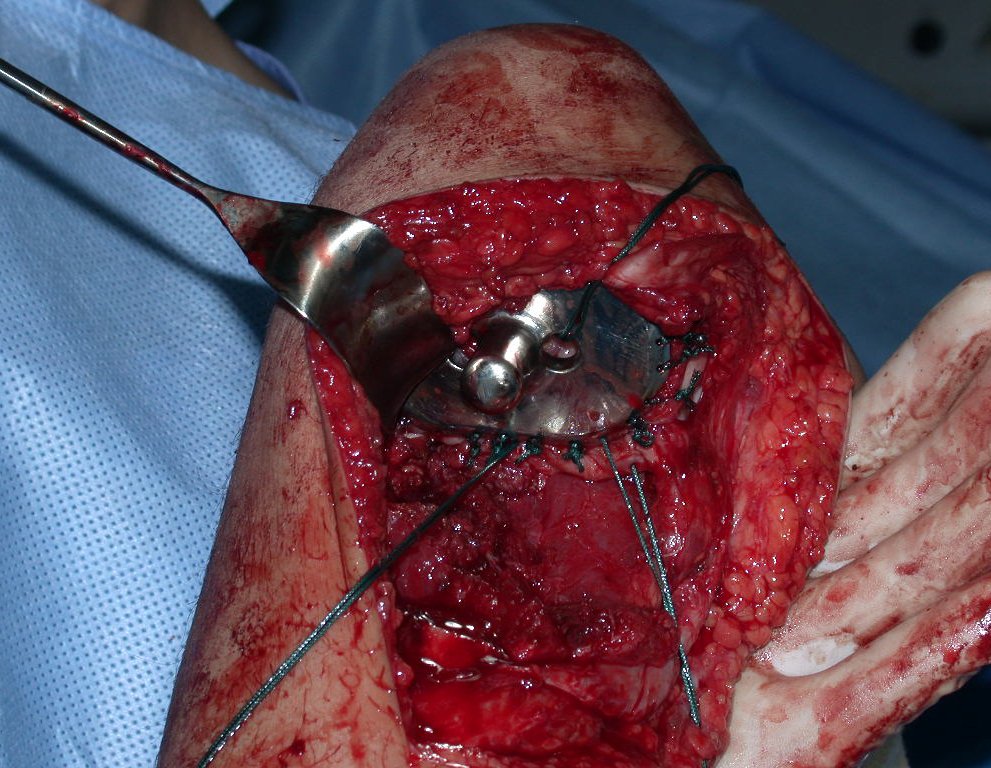
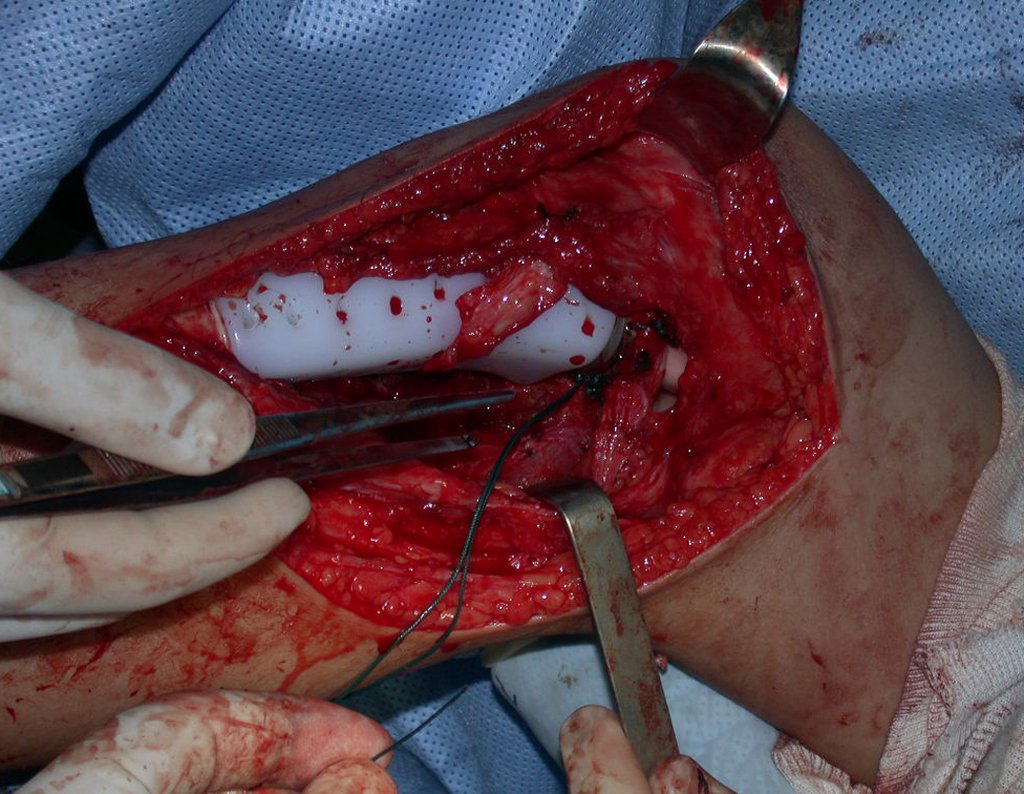
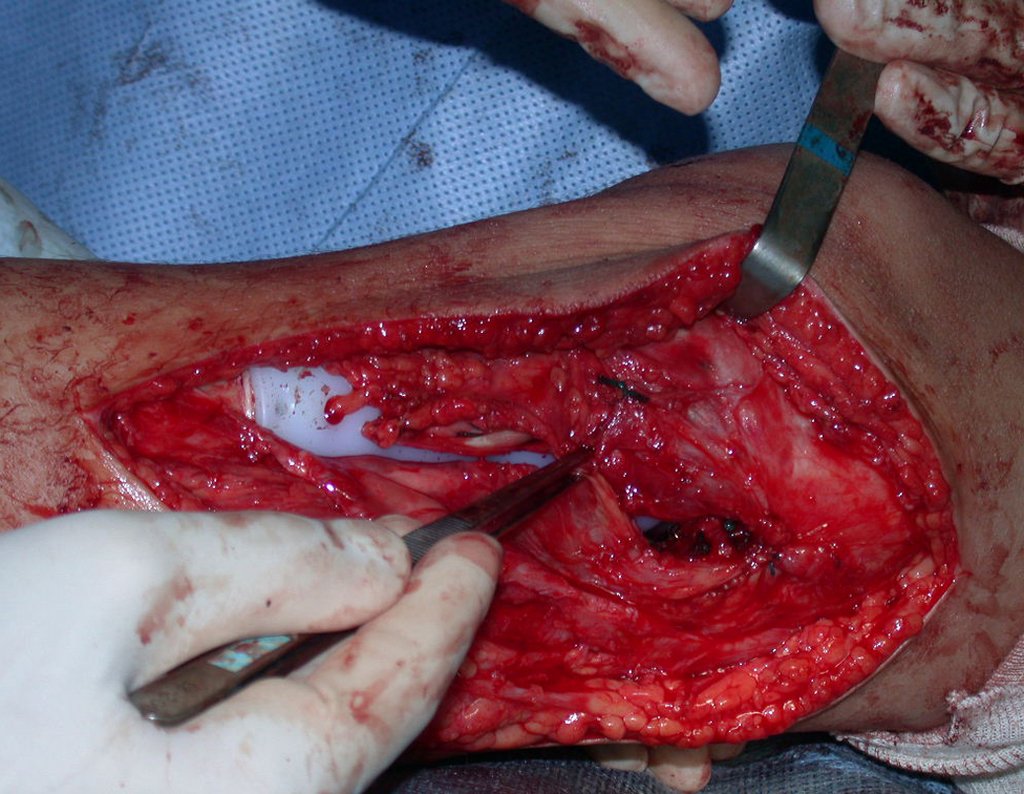
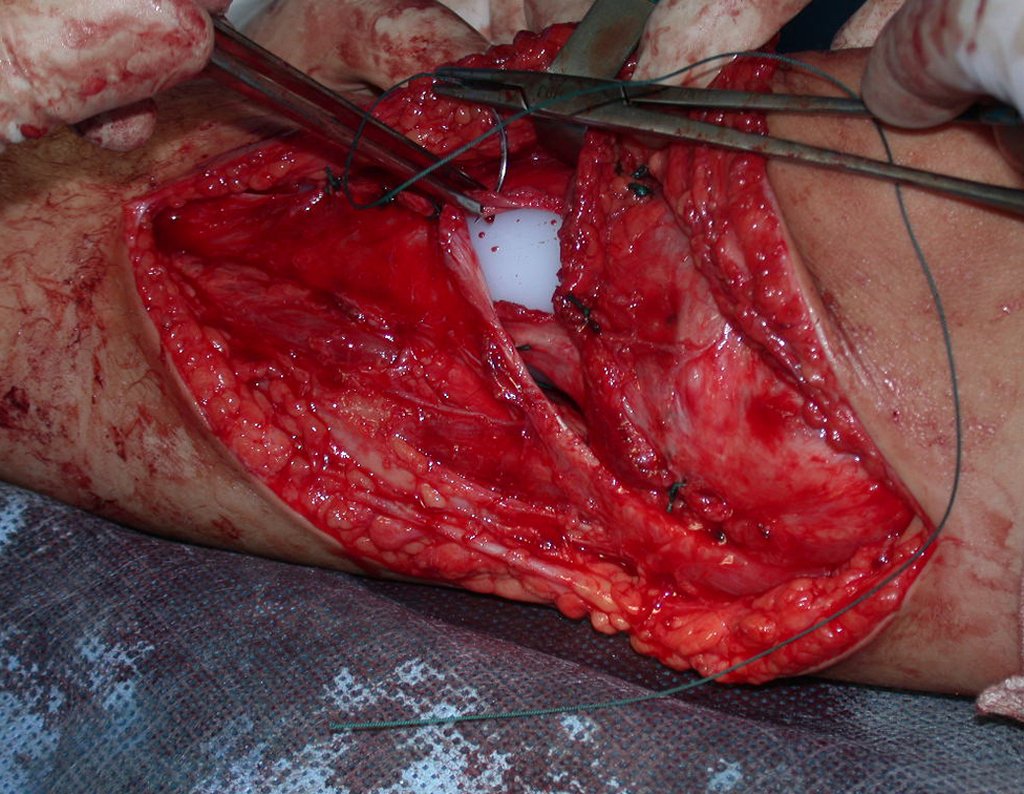
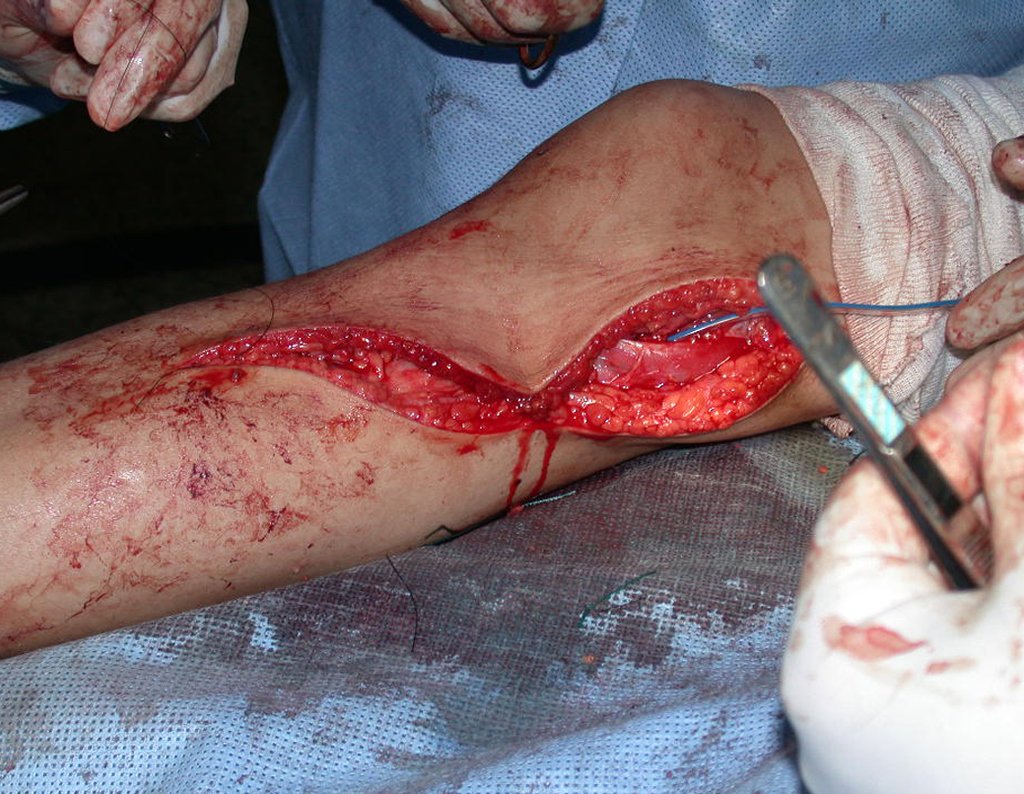
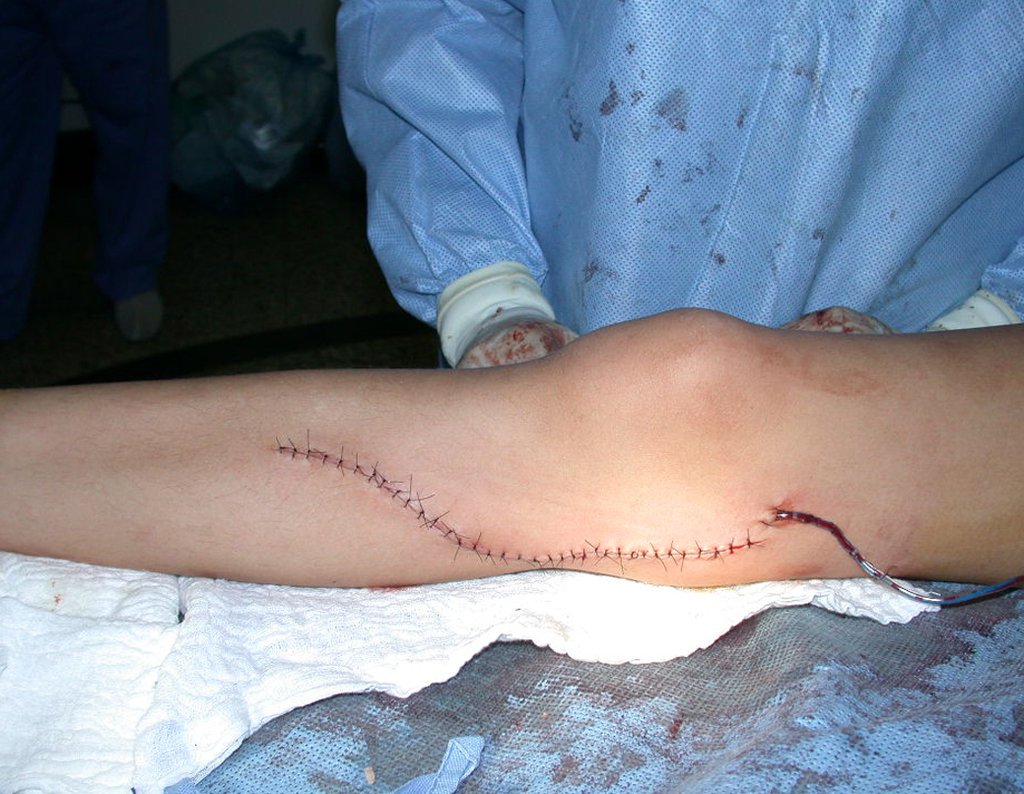
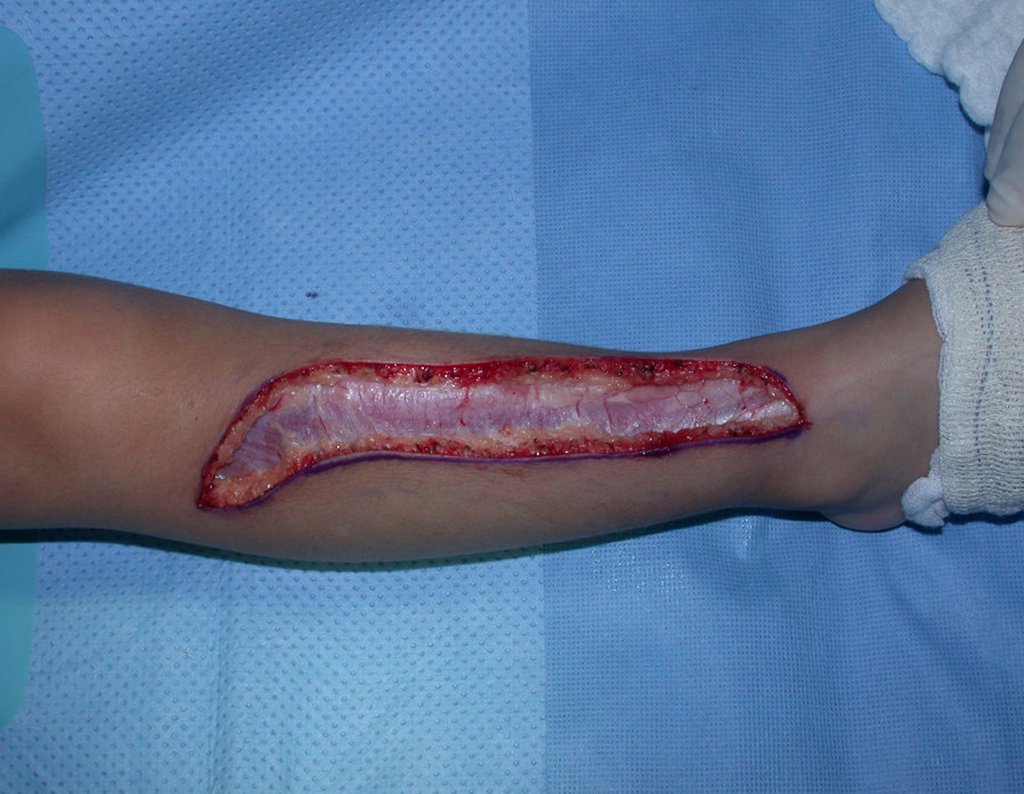
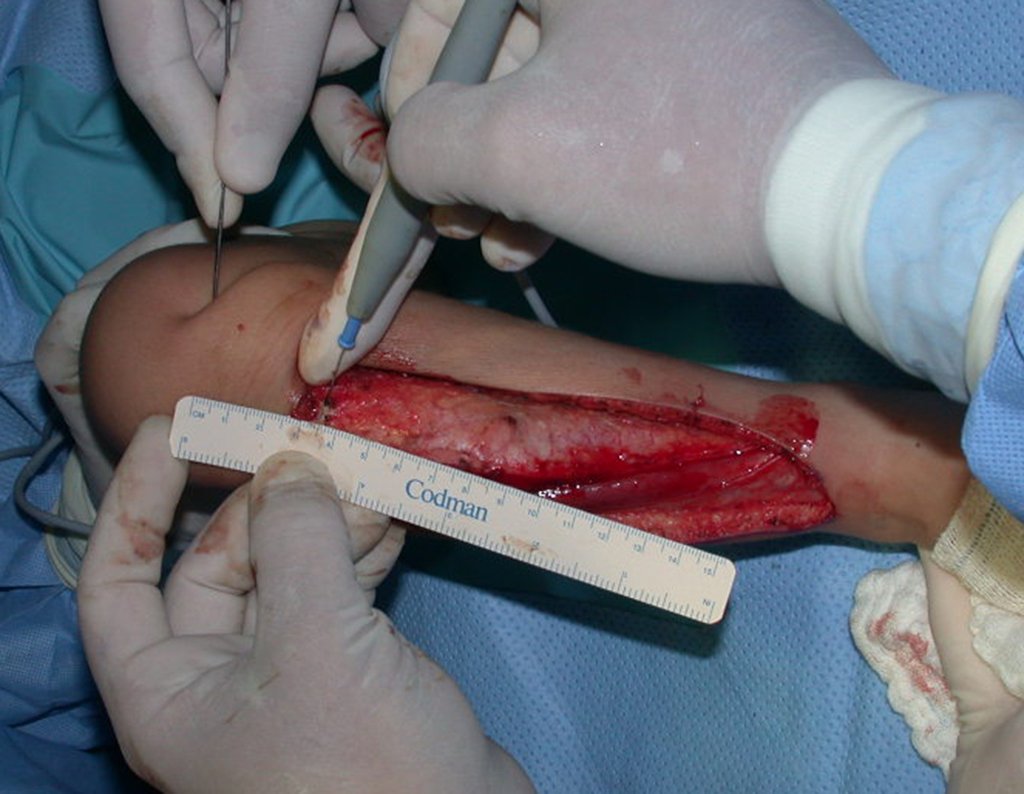
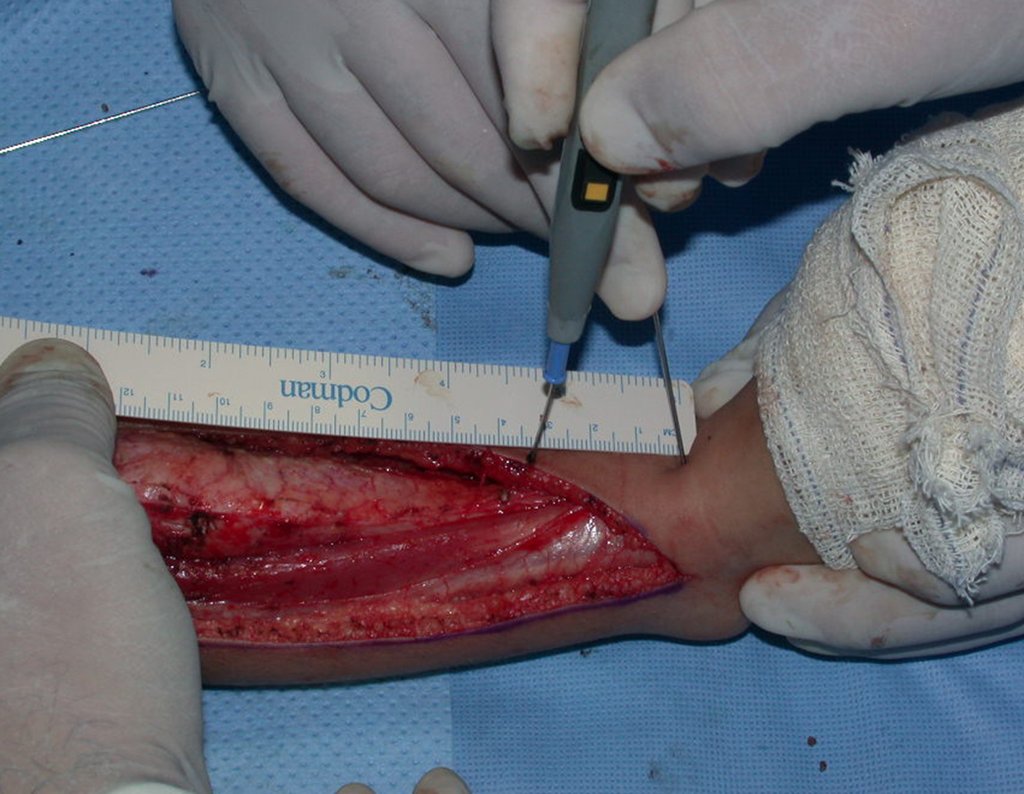
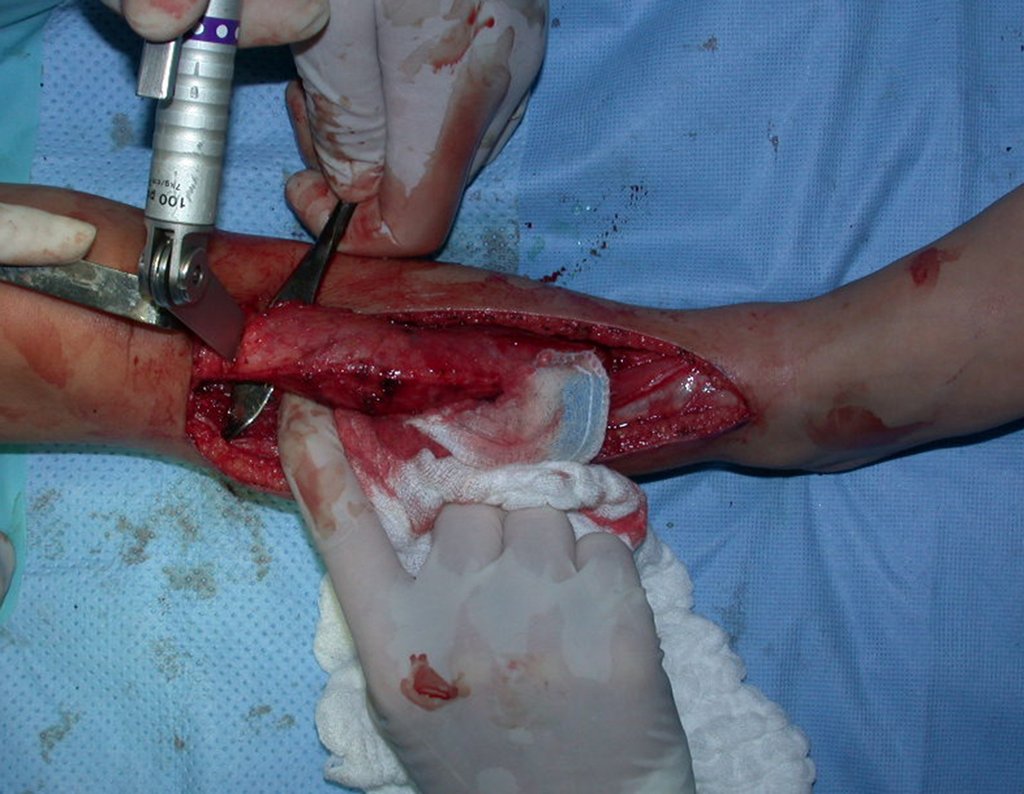
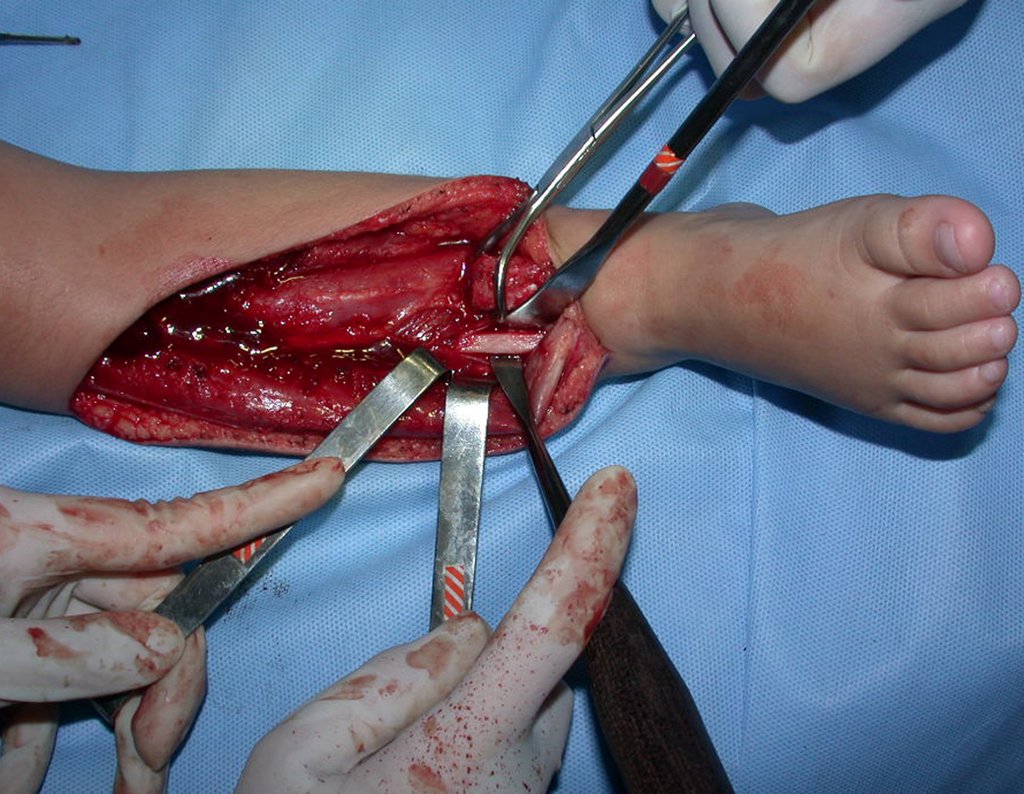
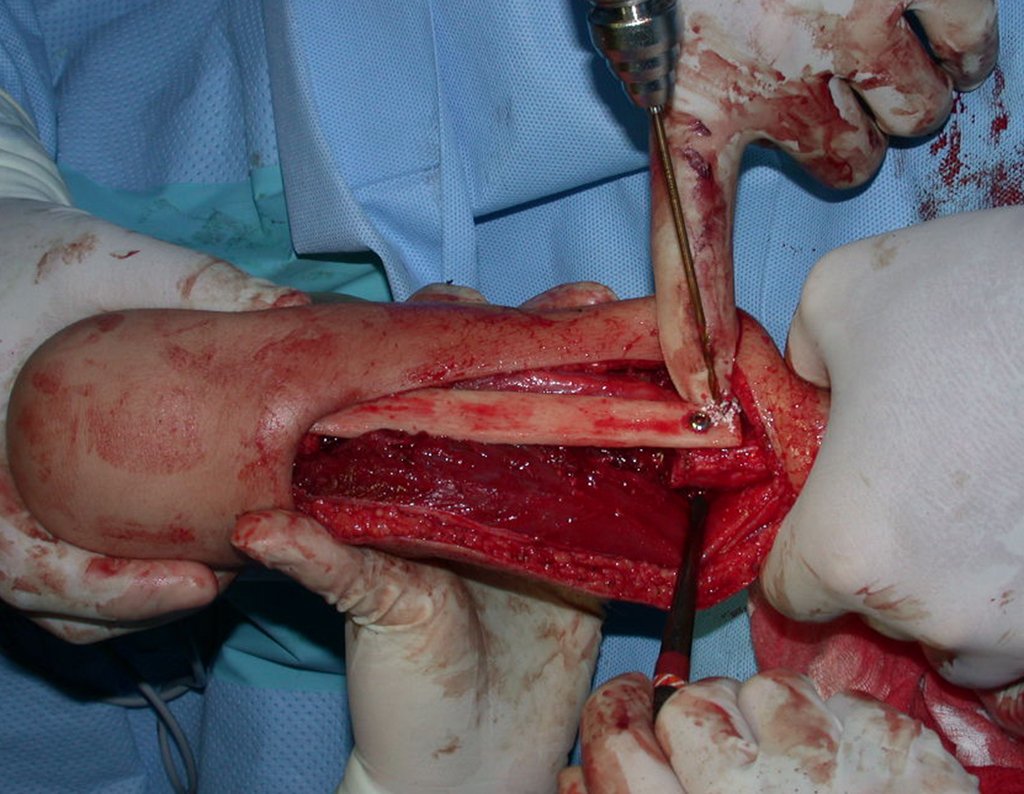
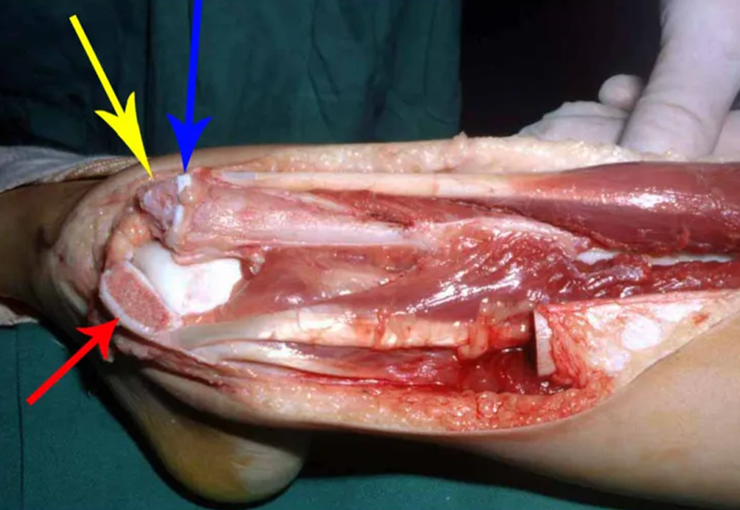
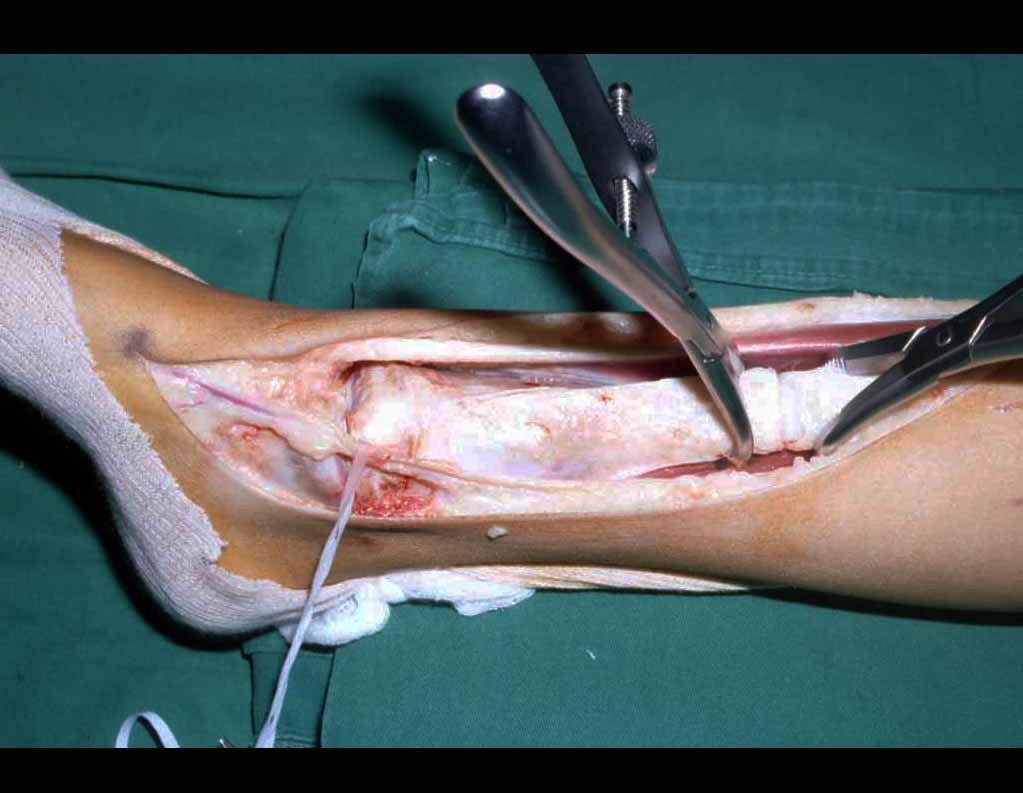
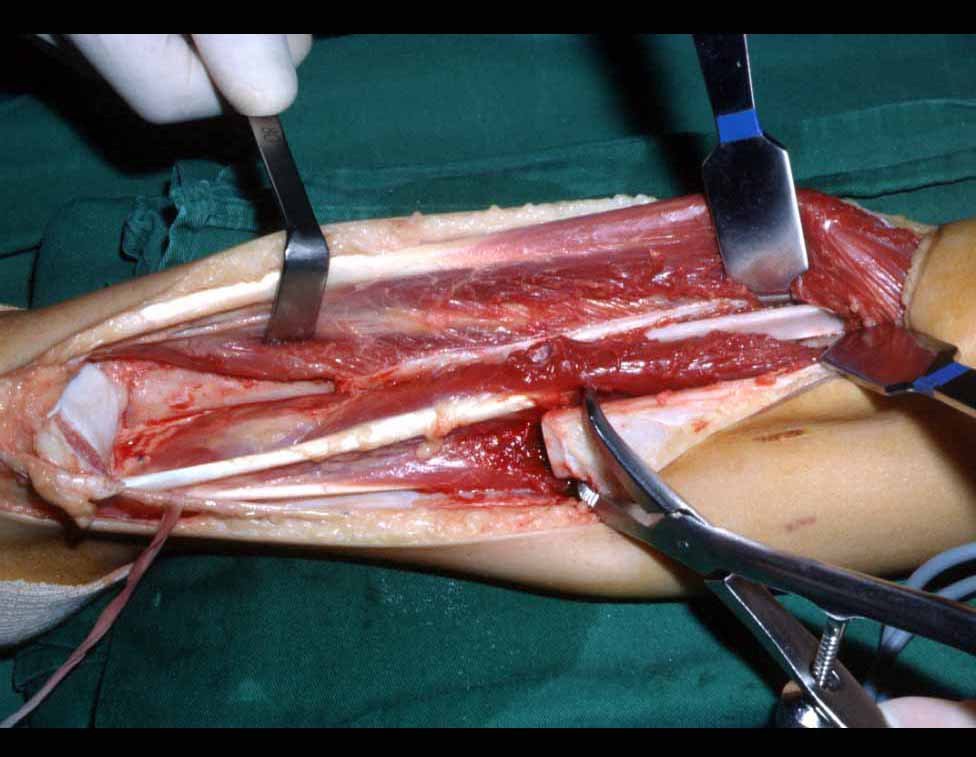
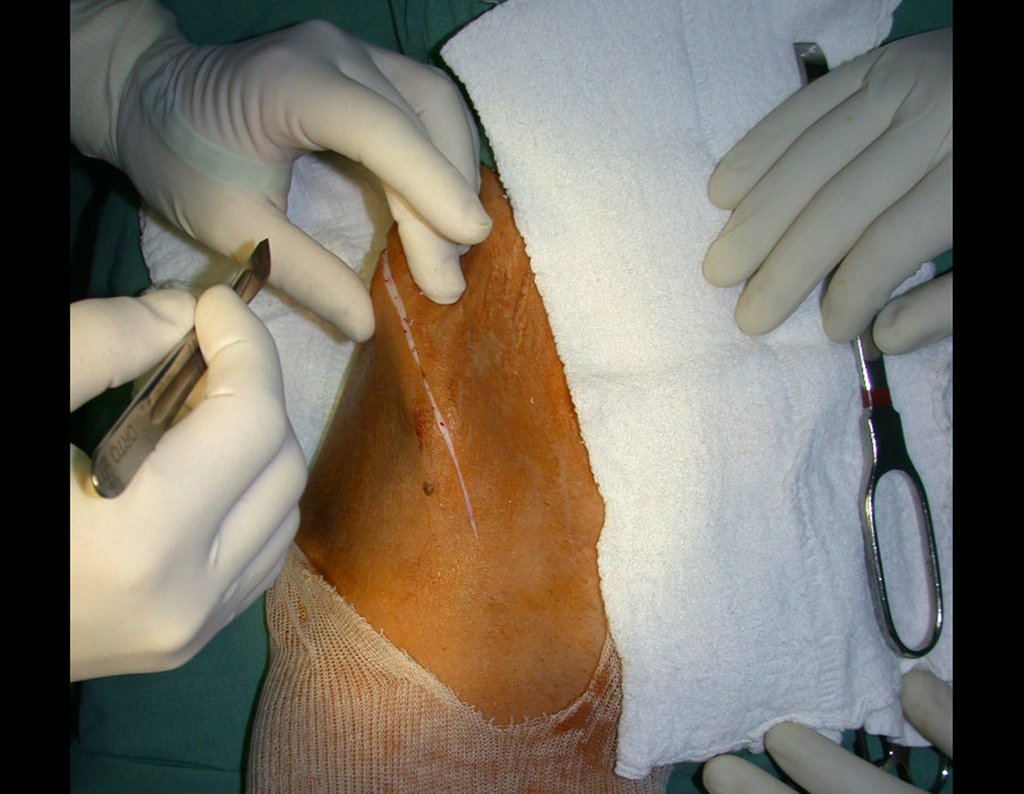
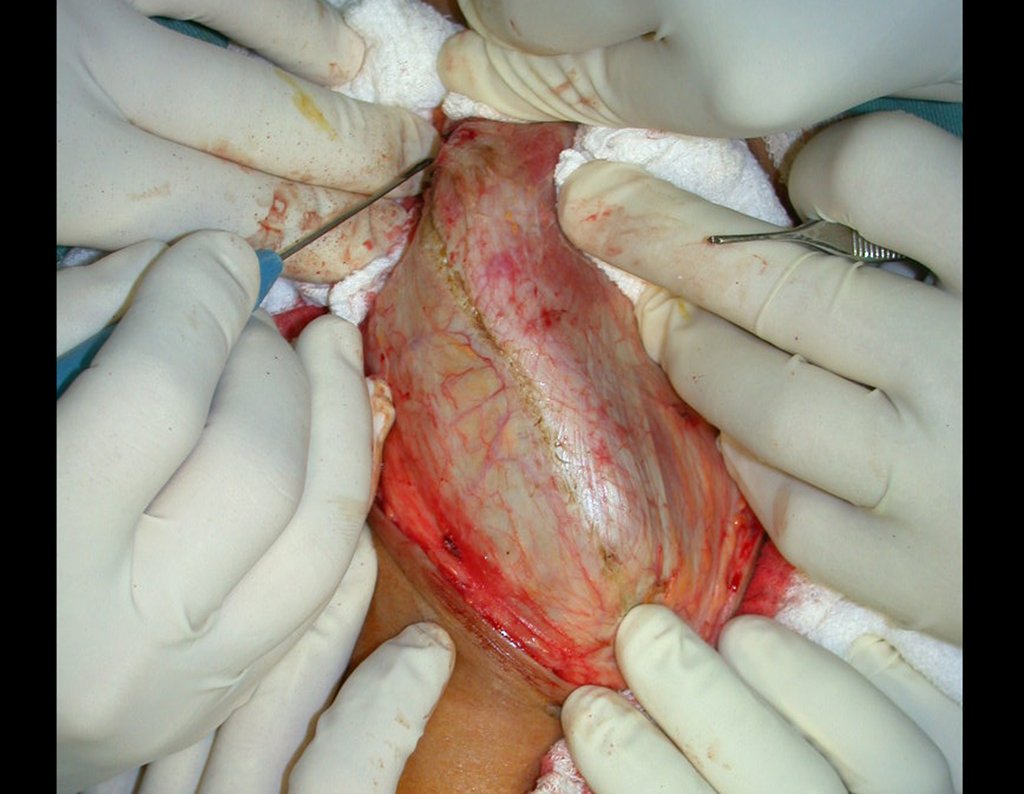
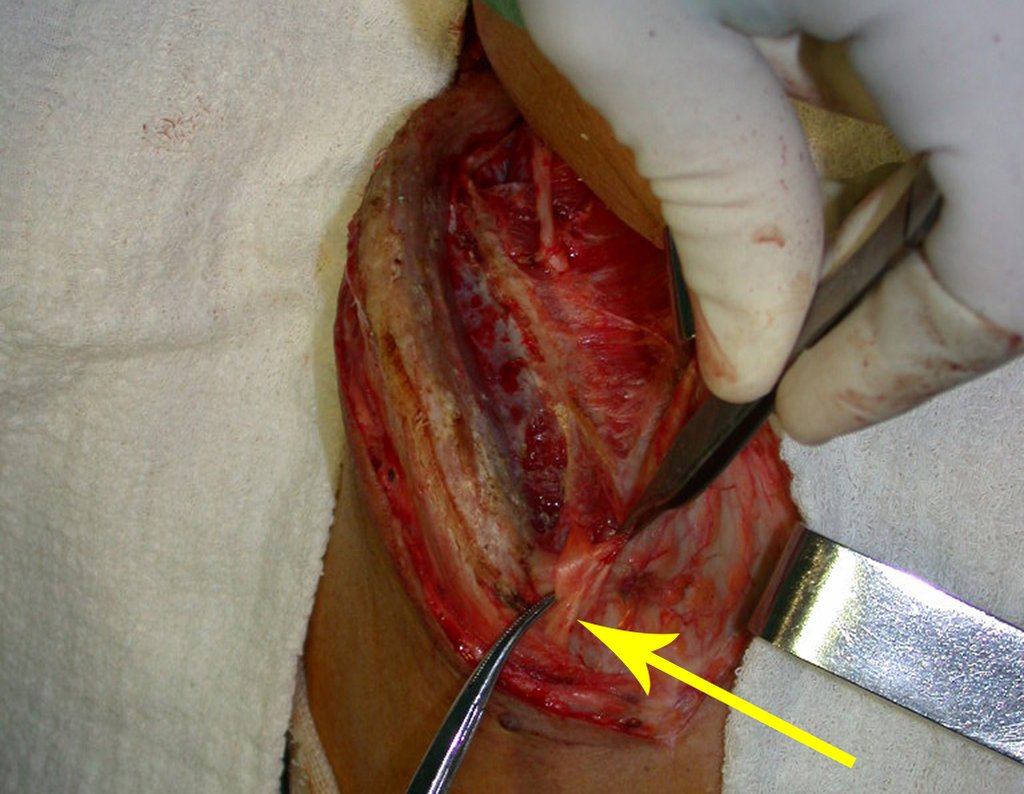
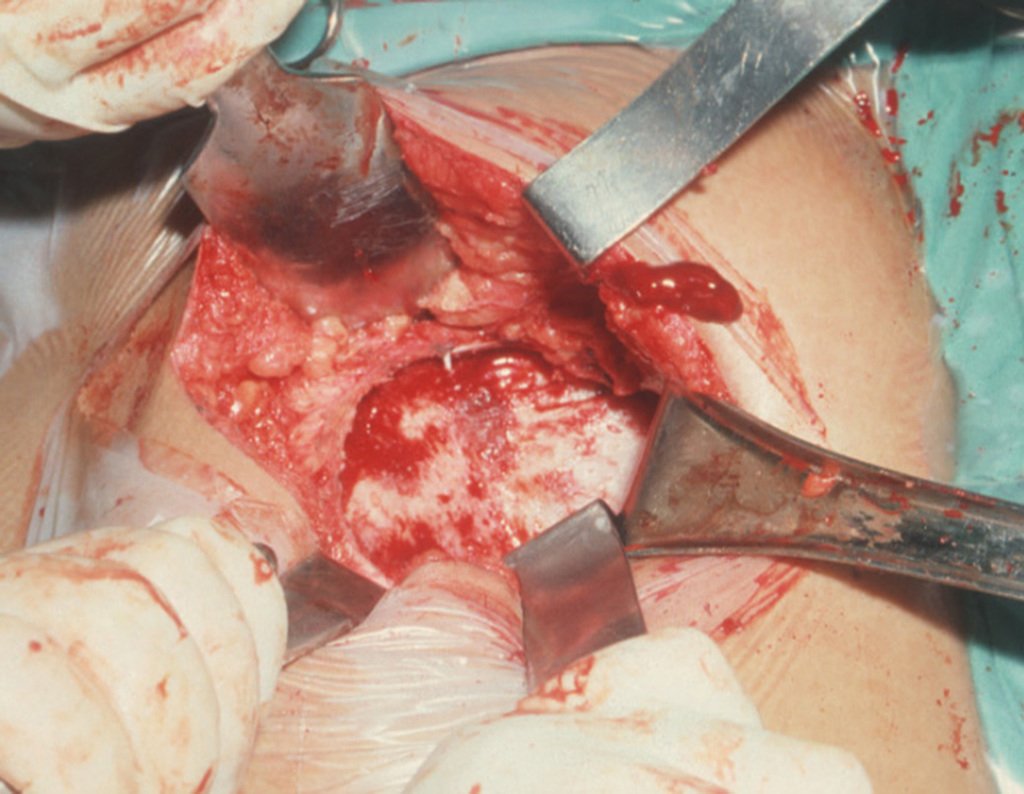
A cirurgia é realizada em decúbito dorsal horizontal, preferentemente sem uso de garroteamento do membro. Os detalhes da ressecção são mostrados nas figuras 38 a 57.


Author: Prof. Dr. Pedro Péricles Ribeiro Baptista
Orthopedic Oncosurgery at the Dr. Arnaldo Vieira de Carvalho Cancer Institute
Office : Rua General Jardim, 846 – Cj 41 – Cep: 01223-010 Higienópolis São Paulo – SP
Phone: +55 11 3231-4638 Cell:+55 11 99863-5577 Email: drpprb@gmail.com